Svante Arrhenius
Svante August Arrhenius (Aussprache: [ˌsvanːtə aˈɹeːniɵs]; * 19. Februar 1859 auf Gut Wik bei Uppsala; † 2. Oktober 1927 in Stockholm) war ein schwedischer Physiker und Chemiker. 1903 erhielt er den Nobelpreis für Chemie. Er wies nach, dass in Wasser gelöste Salze als Ionen vorliegen. Die Salze zerfallen im Wasser vielfach nicht vollständig in Ionen, sondern nur – abhängig von der Konzentration – zu einem bestimmten Prozentsatz; Arrhenius prägte hierfür das Wort Aktivitätskoeffizient. 1896 sagte er als Erster eine globale Erwärmung aufgrund der anthropogenen Kohlendioxid-Emission voraus.[1][2]

Leben
Svante August Arrhenius wurde als Sohn von Svante Georg Arrhenius (1813–1885) und seiner Frau Carolina Christina (geb. Thunberg) (1820–1906) auf dem Gut Wik am Mälarsee geboren. Der Vater arbeitete zunächst als Landvermesser und wurde später „Akademievogt“ an der Universität Uppsala, an welcher er selbst studiert hatte. Die schlechte Bezahlung dieses Postens ließ ihn zusätzlich die Stelle des Verwalters auf dem Gut unweit von Uppsala annehmen. Der junge Svante verbrachte dort jedoch nur eine kurze Zeit, Anfang der 1860er Jahre zog die Familie nach Uppsala. Der Lohn des Vaters war aufgebessert worden und machte die zweite Anstellung als Verwalter überflüssig.
Schulische und akademische Ausbildung
Svante August war ein ungewöhnlich begabtes Kind. Bereits im Alter von drei Jahren lernte er das Lesen und wurde in der Folgezeit ein ausgezeichneter Kopfrechner. Mit acht Jahren besuchte er die Domschule zu Uppsala, wo er sich besonders in Mathematik und Physik hervortat. 1876 legte Arrhenius sein Abitur ab und begann ein Studium der Mathematik und Naturwissenschaften an der Universität Uppsala. Zu dieser Zeit lehrte dort Tobias Robert Thalén Physik. Das Verhältnis von Arrhenius zu seinem Lehrer gestaltete sich als schwierig, was einer der Gründe war, weshalb er 1881 an die Universität Stockholm wechselte. Dort lernte er bei Erik Edlund, der seinen talentierten Schüler schon bald förderte. 1884 promovierte Arrhenius mit der in französischer Sprache abgefassten Doktorarbeit Recherches sur la conductibilité galvanique des électrolytes.[3] Diese hatte bereits Arrhenius’ großes Thema zum Inhalt, die elektrolytische Dissoziation.
Die Naturwissenschaftler konnten sich damals jedoch nicht vorstellen, dass in wässrigen Lösungen freie, ungebundene Atome (mit einer entsprechenden Ladung) vorhanden sein könnten. Kochsalz (Natriumchlorid) bestand „aus Chlor und Natrium“. Natrium- und Chloratome seien hochreaktiv und es erschien damals höchst unwahrscheinlich, dass sich diese Atome frei in der Lösung bewegen könnten, da sich der Geruch von Chlor ja hätte nachweisen lassen müssen.
Obwohl die Beurteilung seiner Dissertation sehr schlecht ausgefallen war und ihm keine Möglichkeit zur weitergehenden Habilitierung eröffnete, gewann seine Theorie dennoch einen gewichtigen Fürsprecher. Wilhelm Ostwald hatte die von Arrhenius gemachten Überlegungen am Polytechnikum zu Riga experimentell bestätigen können und kam persönlich nach Stockholm, um den jungen Wissenschaftler kennenzulernen. Ostwald bot Arrhenius eine Professur in Riga an, die dieser wegen einer schweren Erkrankung seines Vaters zunächst nicht annehmen konnte.
Weiterer Weg


Schon bald erhielt Svante Arrhenius ein großzügiges Reisestipendium der Schwedischen Akademie der Wissenschaften, das ihn in den nächsten Jahren durch weite Teile Europas führte. Zunächst folgte er Ostwald nach Riga (1885) und arbeitete anschließend ab 1886 bei Friedrich Kohlrausch in Würzburg, wo er auch mit dessen Doktoranden Walther Nernst bekannt wurde. Seit diesem Besuch erschloss sich der Physiker Kohlrausch weite Bereiche einer neuen physikalischen Chemie.
Dann führte ihn sein Weg zu Ludwig Boltzmann nach Graz (1887) und weiter zu van ’t Hoff nach Amsterdam, anschließend wiederum zu Ostwald, der inzwischen in Leipzig lehrte (beides 1888). Nach einem kurzen Aufenthalt in seiner Heimat arbeitete Arrhenius 1889/90 erneut in Leipzig an Ostwalds Physikalisch-chemischem Institut und Graz. Diese Stationen beschlossen das mehrjährige Wanderleben, denn 1891 nahm Arrhenius eine Stelle als „Laborator für Physik“ an der Universität Stockholm an.
Eine Professur in Gießen, die ihm ebenfalls angetragen worden war, schlug er aus. 1895 wurde sein Posten in eine Professur umgewandelt, die er 1905 – inzwischen bereits mit dem Nobelpreis für Chemie (1903) ausgezeichnet – zu Gunsten des Nobelinstituts für Physikalische Chemie aufgab.
Lebensende
Im höheren Alter war Arrhenius aufgrund seiner zahlreichen Ämter gezwungen, viel Aufwand in Verwaltungsaufgaben zu investieren. Um sich dennoch der Forschungs- und Publikationsarbeit widmen zu können, schonte er seine zeitlebens robuste Gesundheit nicht. Für die Arbeit an einer Neuauflage von Das Werden der Welten stand er beispielsweise im Herbst 1925 täglich um vier Uhr auf. Ende des Jahres erlitt er jedoch einen Schwächeanfall, von dem er sich nicht mehr ganz erholte. Im Frühjahr 1927 trat Arrhenius als Direktor des Nobelinstituts zurück und verfasste im Sommer seine unvollendet gebliebenen Lebenserinnerungen. Ende September kämpfte er mit einem akuten Darmkatarrh, dessen Folgen er am 2. Oktober 1927 erlag. Beigesetzt wurde er seinem Wunsch entsprechend in Uppsala, der Stadt seiner Jugend.
Nachkommen
Arrhenius war zweimal verheiratet. Seine erste Frau wurde 1894 Brita Maria Margareta Sophia Rudbeck. Mit ihr hatte er einen Sohn: Olof Arrhenius (* 2. November 1895; † 8. Mai 1977), Biochemiker. Die Ehe wurde aber schon 1896 geschieden. Seine zweite Frau wurde 1905 Maria Johansson (1871–1957). Das Paar hatte den Sohn Sven (1909–1991) und zwei Töchter.
Wissenschaftliches Werk
Arrhenius war ein sehr vielseitiger Wissenschaftler, der auf so unterschiedlichen Gebieten wie physikalischer Chemie, Meteorologie, Geophysik, Physiologie und Kosmologie forschte. Als seine bedeutendste Leistung ist die Ausarbeitung der Grundlagen der elektrolytischen Dissoziation anzusehen.
Elektrolytische Dissoziation
Arrhenius machte sich insbesondere um die Theorie der elektrolytischen Dissoziation verdient.
Die Arbeiten von van ’t Hoff, mittels derer er durch Messung der ebullioskopischen Eigenschaften in Flüssigkeiten z. B. Dampfdruckerhöhung und Absenkung des Gefrierpunktes bei Säuren, Basen und Salzen Abweichungen zu einem berechneten molekularen Zusammensetzung gefunden hatte, bestätigten die Theorie von Arrhenius. Richard Abegg konnte durch genaue Messungen von wässrigen Rohrzucker- und Kaliumchloridlösungen nachweisen, dass Kaliumchlorid tatsächlich in Ionen dissoziiert sein musste und die Dissoziationswerte aus Gefrierpunktserniedrigungen gut mit den Leitfähigkeitsmessungen bei gleichen Konzentrationen übereinstimmten.[4]
Nach Kenntnis dieser Schriften fertigte Arrhenius einen kurzen Artikel zur Darlegung der Dissoziationstheorie an.[5] In dieser Arbeit gebrauchte Arrhenius statt des Wortes Dissoziationskoeffizient auch das Wort Aktivitätskoeffizent. Die dissoziierten Spaltprodukte eines Salzes sind die Ionen und der Aktivitätskoeffizient gibt den Anteil der Ionen im Verhältnis zu allen Teilchen dieser Sorte an. Arrhenius kommt aus den Leitfähigkeitsmessungen weiter zum Schluss, dass in sehr großer Verdünnung der Aktivitätskoeffizient gegen 1 strebt und somit in hochverdünnten Lösungen alle Salze, Säuren, Basen vollständig in Ionen dissoziiert sind. Bei konzentrierten Lösungen ist der Aktivitätskoeffizient kleiner als 1, d. h., nicht alle Salzteilchen, Säuren, Basen sind in Ionen dissoziiert.
Arrhenius gab für Leitfähigkeitsmessungen eine einfache Formel zur Bestimmung des Dissoziationsgrades für 1,1-Elektrolyte an:
Dabei ist der Dissoziationsgrad (Aktivitätskoeffizient) des Salzes (der Säure, Base), die molare Äquivalentleitfähigkeit, die Grenzleitfähigkeit bei unendlicher Verdünnung.
Arrhenius nahm ferner an, dass jedem Ion im Salz ein besonderer, individueller Leitfähigkeitscharakter zukommt. Bei Salzmischungen muss dieser besondere Leitfähigkeitscharakter jedes Ions bestimmbar sein. Diese Regel kennen wir heute als die Grenzleitfähigkeit der Ionen bei unendlicher Verdünnung.
Kinetik
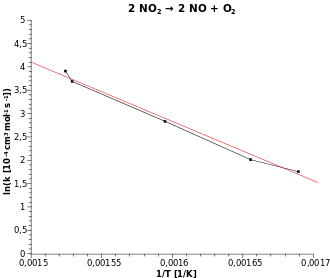
Die Abhängigkeit der Leitfähigkeit von Elektrolyten mit der Temperatur war zwar schon von Kohlrausch nach dessen erstem Treffen mit Arrhenius gründlich untersucht worden, aber er konnte feststellen, dass manche Elektrolyte bei Temperaturerhöhung mit einer Abnahme der Leitfähigkeit reagieren.
Die Beeinflussung der Reaktionsgeschwindigkeit durch die Konzentrationen der beteiligten Ionen und Temperatur war ein weiteres Thema seiner Arbeiten 1889. Die Temperatur beeinflusst exponentiell die Reaktionsgeschwindigkeit von Ionen, deren Konzentration er durch Leitfähigkeitsmessungen kontrollieren konnte. Die Auswertemethodik mittels Arrhenius-Gleichung ist allgemein anerkannt.
Meteorologie und Geophysik
Arrhenius forschte aber auch zu Themen der Atmosphäre und Meteorologie wie zum Beispiel über das Polarlicht, Gewitter und Klimaschwankungen. Er vermutete, dass kosmischer Strahlungsdruck über den Raum transportiert wird und so zu Lichterscheinungen wie dem Polarlicht führt. Er stellte im Jahr 1895 eine Theorie zum Treibhausgaseffekt vor. Kohlenstoffdioxid könnte die infraroten Wärmestrahlen des von der Erde abgestrahlten Lichts absorbieren und durch viel Kohlenstoffdioxid könnte sich das Erdklima aufheizen. Insbesondere durch Verbrennung fossiler Energieträger wie Kohle, Öl und Gas könnte sich der Kohlendioxidgehalt der Atmosphäre erhöhen, so dass es zu einem Temperaturanstieg kommen könne. Auch nahm er an, dass der Gehalt an Wasserdampf in der Atmosphäre in eine gleiche Richtung wie Kohlenstoffdioxid wirke und so das Resultat verstärken könne. Er rechnete damit, dass eine Verdoppelung der Kohlenstoffdioxid-Konzentration in der Atmosphäre zu einer weltweiten Temperaturerhöhung von 5 °C führen werde.[6] Die Vegetation sollte seiner Meinung nach als Kohlendioxidregulator wirken. In der Forschungsgeschichte des Klimawandels nimmt er daher einen wichtigen Platz ein. Er gewann dem menschlichen, verstärkenden Einfluss auf den Treibhauseffekt überwiegend positive Seiten ab:
„Schon die für Industriezwecke benötigte Kohleverbrennung ist geeignet, den Kohlensäuregehalt der Luft merkbar zu vermehren. Außerdem scheint der Vulkanismus ... sich im Steigen zu befinden. ... Man hört oft Klagen darüber, daß die in der Erde angehäuften Kohlenschätze von der heutigen Menschheit ohne Gedanken an die Zukunft verbraucht werden; und man erschrickt bei den furchtbaren Verwüstungen an Leben und Eigentum, die den heftigen vulkanischen Ausbrüchen in unserer Zeit folgen. Doch kann es vielleicht zum Trost gereichen, daß es hier wie so oft keinen Schaden gibt, der nicht auch sein Gutes hat. Durch Einwirkung des erhöhten Kohlensäuregehaltes der Luft hoffen wir uns allmählich Zeiten mit gleichmäßigeren und besseren klimatischen Verhältnissen zu nähern, besonders in den kälteren Teilen der Erde; Zeiten, da die Erde um das Vielfache erhöhte Ernten zu tragen vermag zum Nutzen des rasch anwachsenden Menschengeschlechtes.“[7]
Physiologie
Arrhenius erforschte mit Mitarbeitern auch die Immunchemie und schrieb darüber ein Buch. Seine Thesen standen jedoch im Widerspruch zu Paul Ehrlichs Ansichten zur Immunchemie.
Kosmogonie und Kosmologie

Arrhenius beschäftigte sich intensiv mit Problemen der Kosmologie. So begründete er 1906 die Panspermie-Lehre, in der die Hypothese vertreten wird, dass das Leben durch Meteoriten auf die Erde gelangt ist. Er glaubte, dass Sporen zwischen Planeten übertragen werden könnten. Diese Idee wurde später vom englischen Astronomen Fred Hoyle erneut aufgegriffen. 1903 veröffentlichte er sein Lehrbuch der kosmischen Physik.
Ehrungen

Arrhenius war Mitglied zahlreicher Akademien und wissenschaftlicher Gesellschaften in Schweden und im Ausland, unter anderem der Königlichen Gesellschaft der Wissenschaften in Uppsala (seit 1899), der Königlichen Physiographischen Gesellschaft in Lund (seit 1900), der Königlich Schwedischen Akademie der Wissenschaften (seit 1901), der Akademie der Wissenschaften zu Göttingen (seit 1901), der Norwegischen Akademie der Wissenschaften (seit 1902), der Königlich Dänischen Akademie der Wissenschaften und der Königlichen Wissenschafts- und Literaturgesellschaft in Göteborg (seit 1903), der Russischen Akademie der Wissenschaften (seit 1903, ab 1925 Ehrenmitglied), der National Academy of Sciences (1908), der American Philosophical Society (1911) sowie der American Academy of Arts and Sciences (1912). 1904 wurde Arrhenius Ehrenmitglied des Vereins Schwedischer Ärzte und 1920 der Königlich Schwedischen Akademie der Ingenieurwissenschaften. Im Jahr 1902 erhielt er die Davy-Medaille der Royal Society. 1911 wurde er korrespondierendes Mitglied der Académie des sciences.
Am 8. August 1903 verlieh die Medizinische Fakultät der Universität Heidelberg Svante Arrhenius die Ehrendoktorwürde. Wenige Wochen später erhielt er „… in Anerkennung des außerordentlichen Verdienstes, das er sich durch seine Theorie über die elektrolytische Dissoziation um die Entwicklung der Chemie erworben hat“ als erster Schwede den Nobelpreis für Chemie. Auch die Universitäten Cambridge, Oxford, Greifswald, Leipzig, Groningen, Edinburgh und Birmingham verliehen ihm Ehrendoktorwürden.
Ein Marskrater, der Mondkrater Arrhenius und der Asteroid (5697) Arrhenius sind nach ihm benannt.[8] Die Schwedische Chemische Gesellschaft verleiht seit 1962 jährlich die Arrhenius-Plakette für herausragende wissenschaftliche Forschung auf dem Gebiet der Chemie.[9]
Schriften

- Recherches sur la conductibilité galvanique des électrolytes. (Abgeschlossen 1883, gedruckt 1884) – Die Doktorarbeit von Arrhenius. Dem wissenschaftshistorisch interessierten Leser ist die Arbeit u. a. durch Ostwalds Klassiker der exakten Wissenschaften (Band 160) zugänglich.
- On the influence of carbonic acid in the air upon the temperature of the ground. The London, Edinburgh and Dublin Philosophical Magazine and Journal of Science 5, 237–276 (1896), online (Memento vom 6. Oktober 2014 im Internet Archive) (deutsch: Über den Einfluss von Kohlensäure in der Luft auf die Bodentemperatur)
- Lärobok i teoretisk elektrokemi. (1900, dt. 1901 Lehrbuch der Elektrochemie, online – Internet Archive)
- Lehrbuch der kosmischen Physik. (1903, 2 Bände, Erster Teil – Internet Archive, Zweiter Teil – Internet Archive)
- Världarnas utveckling (1906)
- (dt. 1908 Das Werden der Welten. Akademische Verlagsgesellschaft Leipzig, übersetzt aus dem Schwedischen von L. Bamberger, online – Internet Archive)
- Die Vorstellung vom Weltgebäude im Wandel der Zeiten. Das Werden der Welten, neue Folge. (1908, online – Internet Archive)
- Immunochemie. Anwendungen der physikalischen Chemie auf die Lehre von den physiologischen Antikörpern. (1907, online – Internet Archive)[10]
- Theorien der Chemie, Leipzig: Akademische Verlagsgesellschaft 1906 (Vorlesungen in Berkeley)
- Das Schicksal der Planeten. Akademische Verlagsgesellschaft, Leipzig 1911.
- Theories of Solutions (1912, online – Internet Archive)
- Quantitative Laws in Biological Chemistry (1915, online – Internet Archive)
- Kemien och det moderna livet. (1919, dt. 1922 Chemie und das moderne Leben).
- Erde und Weltall (1926).
Literatur
- Günther Bugge (Hg.): Das Buch der grossen Chemiker. Band 2: Von Liebig bis Arrhenius. Verlag Chemie, Berlin 1930 (6. unveränderter Nachdruck. Verlag Chemie, Weinheim u. a. 1984, ISBN 3-527-25021-2). (Die zwanzig Seiten umfassende Arrhenius-Biografie in diesem Band wurde von Wilhelm Palmaer, einem ehemaligen Schüler Arrhenius’, geschrieben. Geeignet für einen Überblick. Gibt bezüglich des Lebenslaufes teils konträre Informationen im Vergleich zum Werk von Riesenfeld).
- Ernst H. Riesenfeld: Svante Arrhenius. Akademische Verlagsgesellschaft, Leipzig 1931. (Arrhenius-Biografie mit neun Abbildungen. Sie bringt dem Leser neben dem Chemiker und seinem Werk auch den Menschen Svante Arrhenius etwas näher. Bezüglich der wissenschaftlichen Bewertung des Werkes von Arrhenius aufgrund des Erscheinungsjahres veraltet).
- Elisabeth Crawford: Arrhenius. From Ionic Theory to the Greenhouse Effect. Science History Publications, Canton MA 1996, ISBN 0-88135-166-0 (Uppsala Studies in History of Science 23), (englisch, 320 Seiten mit vielen Literaturverweisen).
- Alois Kernbauer: Svante Arrhenius’ Beziehungen zu österreichischen Gelehrten. Publikationen aus dem Archiv der Universität Graz 21, Graz 1988.
Weblinks
- Informationen der Nobelstiftung zur Preisverleihung 1903 an Svante Arrhenius (englisch)
- Literatur von und über Svante Arrhenius im Katalog der Deutschen Nationalbibliothek
- Zeitungsartikel über Svante Arrhenius in der Pressemappe 20. Jahrhundert der ZBW – Leibniz-Informationszentrum Wirtschaft
- Der Nobelpreis – Svante August Arrhenius
Einzelnachweise
- Rahmstorf, Stefan; Schellnhuber, Hans-Joachim (2012): Der Klimawandel. Diagnose, Prognose, Therapie. 7., vollständig überarbeitete und aktualisierte Aufl. München: Beck (Beck'sche Reihe, 2366 : Wissen). Seite 29.
- Svante Arrhenius: On the Influence of Carbonic Acid in the Air upon the Temperature of the Ground. In: Philosophical Magazine and Journal of Science Series 5, Volume 41, April 1896, pages 237-276. Abgerufen am 9. August 2019 (englisch).
- Lebensdaten, Publikationen und Akademischer Stammbaum von Svante August Arrhenius bei academictree.org, abgerufen am 1. Januar 2018.
- Richard Abegg: Gefrierpunktserniedrigungen sehr verdünnter Lösungen. In: Z. phys. Chem. Band 20, Nr. 2, 1896, S. 207–233.
- Ueber die Dissociation der in Wasser gelösten Stoffe. Zeitschrift für physikalische Chemie, 1. Jg., Nr. 11–12, 1887, S. 631–648.
- Tim Staeger: Der Vater des Treibhauseffekts. In: wetter.tagesschau.de. 23. November 2018, abgerufen am 7. Februar 2019.
- Svante Arrhenius: Das Werden Der Welten. BoD – Books on Demand, 2012, ISBN 978-3-86444-678-8, S. 56–57 (google.de [abgerufen am 11. Mai 2021]).
- Arrhenius (6766 P-L) JPL Small-Body Database Browser (abgerufen am 1. April 2010).
- Arrhenius-plaketten. Svenska Kemisamfundet, abgerufen am 6. September 2019.
- übersetzt aus dem Englischen: Immunochemistry. (1907, online – Internet Archive)