Paraformaldehyd
Paraformaldehyd (PFA) ist das kurzkettige Polymer des Formaldehyds, der Polymerisationsgrad beträgt 8–100.[1] Es handelt sich um ein weißes Pulver, das bei niedrigem pH-Wert oder unter Erhitzung wieder in Formaldehyd aufgespalten wird. Der Abbau erfolgt dabei über die Endgruppen. Werden diese durch eine Veresterung oder Veretherung geschützt, so wird ein stabiler Kunststoff erhalten, das Polyoxymethylen.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
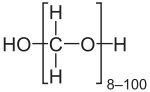 | ||||||||||
| Allgemeines | ||||||||||
| Name | Paraformaldehyd | |||||||||
| Andere Namen |
| |||||||||
| CAS-Nummer | 30525-89-4 | |||||||||
| Monomer | Formaldehyd | |||||||||
| Summenformel der Wiederholeinheit | CH2O | |||||||||
| Molare Masse der Wiederholeinheit | 30,03 g·mol−1 | |||||||||
| Kurzbeschreibung |
weißer Feststoff mit charakteristischem Geruch [1] | |||||||||
| Eigenschaften | ||||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
1,39 g·cm−3 (20 °C)[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
schwer löslich in Wasser (20 °C)[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Toxikologische Daten | ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Beim Erhitzen von Paraformaldehyd in Wasser oder einer wässrigen Pufferlösung zerfällt es, man erhält eine Formaldehydlösung. Diese wird manchmal als „Paraformaldehydlösung“ bezeichnet, um sie von Formaldehydlösungen abzugrenzen, die durch Verdünnung aus Formalin entstanden sind, einer konzentrierten Formaldehydlösung, die zur Stabilisierung auch Methanol enthält. Strenggenommen ist die Bezeichnung Paraformaldehydlösung jedoch falsch, da das Polymer in Wasser unlöslich ist. Diese Lösung wird in der Biologie für die Fixierung von Geweben oder Zellkulturen verwendet, in der Regel in Konzentrationen zwischen 0,5 %[3] und 4 %,[4] gepuffert auf neutralen pH-Wert. Die Wirkung beruht auf der reversiblen Vernetzung von Proteinen.
Paraformaldehyd ist gesundheitsschädlich und steht im Verdacht, krebserregend zu sein. Der orale LD50-Wert für eine Ratte liegt bei 592 mg/kg. Der Dampfdruck bei 25 °C liegt bei 2hPa.[1] Die Maximale Arbeitsplatzkonzentration beträgt 0,3 ml·m−3 bzw. 0,37 mg·m−3.[1]
In der präparativen Chemie kann Paraformaldehyd für Formylierungsreaktionen und davon abgeleitete Synthesen Anwendung finden, z. B. Mannich-Reaktion, Blanc-Reaktion („Chlormethylierung“).
Siehe auch
- Polyoxymethylen – chemisch identischer technischer Kunststoff
- Paraldehyd
Einzelnachweise
- Eintrag zu Paraformaldehyd in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. Juli 2017. (JavaScript erforderlich)
- Datenblatt Paraformaldehyd (PDF) bei Merck, abgerufen am 5. April 2014.
- Howard M. Shapiro: Practical Flow Cytometry. 4. Ausgabe, John Wiley & Sons, 2005. ISBN 978-0-471-43403-0. S. 304.
- Alan Michael Tartakoff: Methods in Cell Biology, Volume 31: Vesicular Transport, Part A: Vesicular Transport. Teil 1, Academic Press, 1989. ISBN 978-0-08-085929-3. S. 444.



