Mikrofilamente
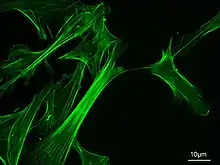
Mikrofilamente sind fadenförmige Protein-Strukturen in eukaryotischen Zellen. Zusammen mit den Mikrotubuli und Intermediärfilamenten bilden sie die Hauptmasse des Cytoskeletts. Sie bestehen hauptsächlich aus dem Protein Aktin und werden daher auch als Aktinfilamente bezeichnet. Die Bezeichnung „Mikrofilament“ rührt daher, dass sie mit einem Durchmesser von nur sieben Nanometern deutlich dünner sind als die Mikrotubuli und Intermediärfilamente. Funktionell spielen sie eine Rolle bei aktiven Bewegungen der Zellen, bei intrazellulären Transportvorgängen und bei der mechanischen Stabilisierung der Zellen.
| Übergeordnet |
| Sarkomer |
| Untergeordnet |
| Aktin Troponin Tropomyosin |
| Gene Ontology |
|---|
| QuickGO |
| Übergeordnet |
| Zytoskelett |
| Untergeordnet |
| Aktin |
| Gene Ontology |
|---|
| QuickGO |
Zusammenbau der Filamente
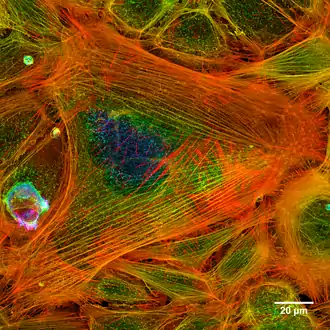
G-Aktin (globuläres Aktin, ein Monomer) bindet das Nucleotid ATP. Dieses Monomer (ATP-Aktin) kann sich nun mit weiteren Aktinmolekülen verbinden – polymerisieren, wobei ATP-Aktin unter Abspaltung (Hydrolyse) eines anorganischen Phosphatrestes zu ADP-Aktin wird. Die entstehende Kette von Aktinmonomeren bildet so die filamentöse Form der Aktinfilamente, auch F-Aktin genannt. Das Filament besteht aus zwei Ketten polymerisierter G-Aktin-Monomere, die sich helixartig umeinanderwinden. Diese Aktin-typische Helixwindung ist regelmäßig nach 7 G-Aktinen zu finden, weshalb man sie auch "Aktinhelix" nennt, um sie z. B. von der DNA-Doppelhelix in ihrer Form zu unterscheiden. Ihr Durchmesser beträgt 7 nm. In der Zelle liegen beide Aktinformen im Gleichgewicht vor, wobei Monomere hauptsächlich im Komplex mit aktinbindenden Proteinen, wie z. B. Profilin, auftreten.[1]
Aktinfilamente weisen eine Polarität auf und haben ein schnell polymerisierendes sogenanntes (+)-Ende und ein langsam polymerisierendes (−)-Ende. ATP-Aktin bindet bevorzugt am (+)-Ende und das Filament wächst an diesem Ende. Das ATP wird in der Folge zu ADP hydrolysiert, wodurch die Bindungsstärke zu den benachbarten Aktinen nachlässt. Am (−)-Ende läuft die Hydrolyse von ATP zu ADP schneller als die Anlagerung eines neuen ATP-Aktins ab, sodass ADP-Aktin dissoziiert und das Filament von dieser Seite verkürzt wird. Aktinmonomere binden aber ATP stärker als ADP, tauschen damit das Nukleotid aus und können wieder am (+)-Ende eingefügt werden. Dieser schnelle Kreislauf ist für die Zellbewegungen wichtig und wird als Treadmilling bezeichnet.[2]
Zahlreiche Begleitproteine steuern die Polymerisations- und Abbauvorgänge. Im Muskel werden die Filamente beispielsweise durch das Tropomyosin stabilisiert, das sich auf ganzer Länge an ein Filament anlegt. In Zellen außerhalb des Herzens und der Skelettmuskulatur wird Caldesmon gebildet.
Bestimmte Proteine bedecken auch die Enden der Aktinfilamente und behindern oder fördern die Verlängerung oder den weiteren Abbau. Andere Proteine verhindern oder fördern die Polymerisation von G-Aktin oder bewirken den Zerfall des F-Aktins.
Beispielsweise setzen sich die Proteine Cofilin und ADF (Aktin depolymerisierender Faktor) an das (−)-Ende und fördern die Dissoziation von Aktin. Das Protein Profilin hingegen fördert den Einbau am (+)-Ende. Die Bindung von sowohl Cofilin als auch Profilin wird über das Aktingebundene Nukleotid (ADP oder ATP) bestimmt.[3]
Auch posttranslationale Modifikationen von Aktin sind an der Polymerisierung beteiligt. So wird jedes fünfte Aktinmonomer in Fibroblasten mit einer Arginylierung versehen, was eine direkte Auswirkung auf die erhöhte Stabilität von Aktinfilamenten hat. Dabei wird vorrangig Beta-Aktin modifiziert .[4]
Der Auf- und Abbau von Aktinfilamenten kann durch Zytoskelett-Inhibitoren gehemmt werden. Ein bakterielles Homolog des Aktins ist FtsA.
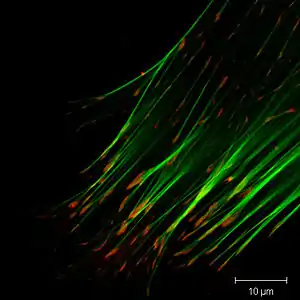
Adapter- und Verbindungsproteine
Eine große Gruppe von Begleitproteinen, die auch als Actin-bindende Proteine (ABP) bezeichnet werden, vernetzt Aktinfilamente untereinander und mit anderen Proteinen. Fimbrin, Villin (Binnengerüst der Mikrovilli), Filamin und Espin bilden Querverbindungen und so mechanisch steife Bündel. α-Actinin bildet ebenfalls Bündel, die typischerweise mit Myosin (siehe unten) verspannt werden. Das Filamin wiederum bildet dreidimensionale Netze (Gele), wie man sie unter der Plasmamembran antrifft.
Actinfilamente strahlen in mehrere Zellkontakte ein, die Adhärens-Kontakte und die Fokalkontakte, aber auch in Tight Junctions. Dabei werden sie über Adaptorproteine an den Proteinstrukturen der Kontakte verankert. Verantwortlich dafür sind unter anderem wieder das α-Actinin, das Vinculin und Talin. Die Proteine der Familie um Ezrin, Radixin, Moesin (ERM-Proteine) vermitteln kurzzeitige und dynamische Bindungen an die Plasmamembran, zum Beispiel bei Änderung der Zellform und aktiver Zellbewegung.
Bestimmte Proteingruppen stellen eine mechanisch stabile Verbindung zwischen dem unter der Plasmamembran liegenden dichten Aktinnetz und der Membran her. Diese wegen verschiedener Erbkrankheiten auch klinisch bedeutsamen Proteine sind die Dystrophine (u. a. im Muskelgewebe, bei Mutationen im Dystrophin-Komplex Muskeldystrophien) und die Spectrine (u. a. verantwortlich für die Form der Erythrozyten, bei Defekt z. B. Kugelzellenanämie). Es handelt sich um lange, dünnere Proteine, die ihre Aufgaben in Komplexen mit zahlreichen anderen Proteinen erfüllen.
Einzelnachweise
- K. C. Holmes, D. Popp, W. Gebhard, W. Kabsch: Atomic model of the actin filament. In: Nature. 347, 1990, S. 21–22. PMID 2395461
- T. D. Pollard, W. D. Earnshaw: Cell Biology. 1. Auflage. Saunders, 2004, ISBN 1-4160-2388-7.
- D. Didry, M. F. Carlier, D. Pantaloni: Synergy between actin depolymerizing factor/cofilin and profilin in increasing actin filament turnover. In: J Biol Chem. 273(40), 1998, S. 25602–25611. PMID 9748225
- M. Karakozova, M. Kozak, C. C. Wong, A. O. Bailey, J. R. Yates, A. Mogilner, H. Zebroski, A. Kashina: Arginylation of beta-actin regulates actin cytoskeleton and cell motility. In: Science. 313(5784), 2006, S. 192–196. PMID 16794040