Tight Junction
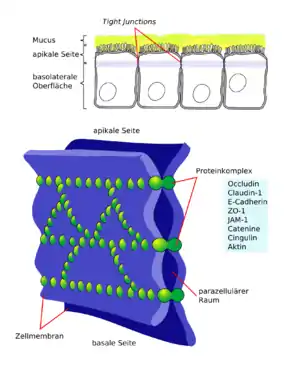
Tight Junctions (engl. für „dichte Verbindung“, lat. Zonula occludens, in deutscher Literatur auch „Schlussleiste“) sind schmale Bänder aus Membranproteinen, die Epithelzellen von Wirbeltieren vollständig umgürten und mit den Bändern der Nachbarzellen in enger Verbindung stehen. Auf diese Weise verschließen die Tight Junctions den Zellzwischenraum und bilden eine parazelluläre Barriere, genannt Diffusionsbarriere, die den Fluss von Molekülen über das Epithel kontrolliert. Außerdem haben sie die Aufgabe, die Polarität der Epithelzellen aufrechtzuerhalten: Sie verhindern, dass Membrankomponenten aus dem apikalen Bereich nach lateral diffundieren und umgekehrt.

Barrierefunktion
Tight Junctions befinden sich im apikalen (der Außenseite näheren) Bereich der seitlichen Zellmembran und stellen dadurch, dass sie die Bänder von benachbarten Zellen aneinanderbinden, einen sehr engen Kontakt zwischen den Membranen zweier benachbarter Zellen her. Diese Kontakte bilden eine Diffusionsbarriere, die den parazellulären Transport von Molekülen über das Epithel verhindert bzw. kontrolliert (Barrierefunktion). Liegen mehrere Tight-Junction-Stränge hintereinander, steigt die Undurchlässigkeit logarithmisch an. Auf diese Weise können Nahrungsaufnahme und Stofftransport in kontrollierter Weise durch die Epithelzellen erfolgen.
Zaunfunktion
Außerdem haben Tight Junctions eine so genannte „Zaun-Funktion“ (fence-function): Sie verhindern die freie Bewegung von Membrankomponenten und erhalten dadurch die Zellpolarität der Epithelzellen, indem sie sie in apikale und basale Bereiche unterteilen. Dies ist von Bedeutung, da z. B. die apikale Zellmembran der Epithelzellen mit den Mikrovilli eine ganz andere biochemische Zusammensetzung aufweist als die basolaterale Membran. Durch die Tight Junctions sind diese voneinander getrennt – eine notwendige Voraussetzung für gerichtete Stofftransporte.
Vorkommen
Tight Junctions kommen in Epithelzellen (z. B. Nieren-, Harnblasen- und Darmepithel) und Gehirnkapillarendothelzellen (Blut-Hirn-Schranke) von Wirbeltieren vor. Bei den Invertebraten nehmen hingegen Septate Junctions eine analoge Funktion wahr.
Aufbau
Die wichtigsten bisher bekannten Membranproteine der Tight Junctions sind die Familie der Claudine sowie das Occludin. Von der Familie der Claudine sind in Wirbeltieren bislang 24 verschiedene bekannt, in anderen Eukaryoten wie zum Beispiel dem Fadenwurm Caenorhabditis elegans sind es vier und in der Taufliege Drosophila melanogaster sieben. Diese integralen Membranproteine sind netzförmig angeordnet und bringen die Membranen zweier Zellen in einer Art Kopf-an-Kopf-Kontakt direkt aneinander. Sie bilden wässrige Poren, die selektiv bestimmte Ionen und Moleküle hindurchlassen, während andere zurückgehalten werden. Die Spezifität der Diffusionbarriere wird dabei durch die unterschiedliche Zusammensetzung der Claudine den jeweiligen Anforderungen, die das Epithel erfüllen muss, angepasst. Ein spezielles Claudin, Claudin 16, welches im Nierenepithel gefunden wurde, ist notwendig, um Mg2+-Ionen aus den Nieren in das Blut aufzunehmen. Eine Mutation in dem Gen, das dieses Protein kodiert, kann zu exzessivem Mg2+-Verlust in den Urin führen. Tight Junctions bilden mal losere (Beispiel: Darm), mal dichtere Barrieren (Beispiel: Blut-Hirn-Schranke). Die Tight Junctions des Dünndarms sind z. B. 10.000-mal durchlässiger für Ionen wie Na+ als die der Harnblase. Die Durchlässigkeit zwischen Epithelzellen kann jedoch auch vorübergehend verändert werden, falls ein erhöhter parazellulärer Transport erwünscht ist. Claudine und Occludine assoziieren mit intrazellulären Membranproteinen, ZO-Proteine nach der Zonula Occludens benannt, welche die Verbindung mit dem Aktin-Cytoskelett herstellen.
Siehe auch
- Zellkontakt Übersicht über die verschiedenen Arten von Zellkontakt
- Adherens junction
- Fokale Adhäsion
- Desmosom
- Hemidesmosom
- Gap junction
Weblinks
- Tight Junction Biology (Memento vom 15. Dezember 2007 im Internet Archive) – Bilder und Texte (englisch)
- Gute Aufnahme eines junctional complex
Literatur
- Alberts, B. et al.: Molecular Biology of the Cell. Garland Science, 4. Auflage, 2002. ISBN 0-8153-4072-9.