Lynestrenol
Lynestrenol ist ein Abkömmling (Derivat) des 19-Nortestosterons. Es gehört zur Stoffgruppe der synthetischen Gestagene und entwickelt durch Verstoffwechselung zum Norethisteron eine progesteronähnliche Wirkung.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
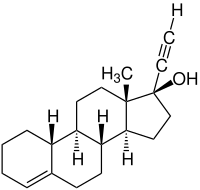 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Lynestrenol | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C20H28O | |||||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 284,44 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||||||||
| Schmelzpunkt |
158–160 °C[2] | |||||||||||||||||||||
| Löslichkeit |
löslich in Chloroform und Ethanol[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Chemisch gehört Lynestrenol zu den Steroiden.
Gewinnung und Darstellung
Zur Synthese von Lynestrenol wird Nortestosteron (1) durch 1,2-Ethandithiol und Bortrifluorid in der 3-Stellung zum Dithioketal (2) umgewandelt und mit Natrium in Ammoniak zum 17β-Hydroxy-estr-4-en (3) reduziert, danach in 17-Stellung mit dem Jones-Reagenz zum Keton (4) oxidiert und mit Lithiumacetylid zum Lynestrenol (5) umgesetzt.[3]
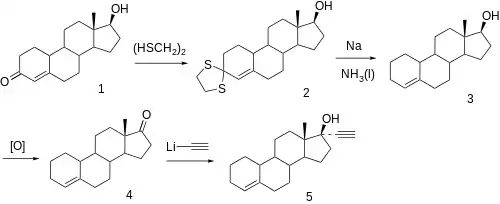
Eigenschaften
Physikalische Eigenschaften
Es handelt sich um einen Feststoff.[2] Der spezifische Drehwert [α]20D beträgt −9,5° bis −11° (3,6 % m/v in 96 % Ethanol).[4]
Chemische Eigenschaften
Lynestrenol besitzt wie die natürlichen Steroidhormone ein Steran-Grundgerüst. Lynestrenol wird synthetisch hergestellt und unterscheidet sich von den natürlichen Steroidhormonen durch das Fehlen einer Ketogruppe am C-3-Atom des Sterangerüstes. Das Molekül ist chiral und besitzt sechs Stereozentren.
Geschichte und Verwendung
Lynestrenol wurde 1969 in die medizinische Therapie eingeführt. Es gehört zu den synthetischen Gestagenen der ersten Generation[5][6] und wurde zur Empfängnisverhütung verwendet – meistens in Kombination mit einem Östrogen (Antibabypille), aber auch allein (Minipille). Heute werden zur Empfängnisverhütung eher moderne Präparate der 3. und 4. Generation verordnet. Ferner ist Lynestrenol zur Behandlung klimakterischer Beschwerden angezeigt (postmenopausale Hormonersatzbehandlung). In den USA gibt es keine zugelassenen Medikamente mit Lynestrenol. Von Bedeutung ist Lynestrenol noch für die Entwicklungsgeschichte der hormonellen Verhütungsmittel (Kontrazeptiva), die sich im Laufe der Jahre verändert und verbessert haben.
Verstoffwechselung
Lynestrenol ist ein Prodrug und wird nach oraler Einnahme im menschlichen Körper zu Norethisteron umgewandelt,[7] welches pharmakologisch aktiv ist.
Fertigarzneimittel
Exluton (D, nicht mehr im Handel), Orgametril (A, NL)
Literatur
- H. Lüllmann, K. Mohr, M. Wehling, L. Hein: Pharmakologie und Toxikologie, Thieme Verlag 2016, 18. Auflage, 476–478. ISBN 978-3-13-368518-4.
Einzelnachweise
- Eintrag zu Lynestrenol bei TCI Europe, abgerufen am 22. Juni 2017.
- The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals, 14. Auflage (Merck & Co., Inc.), Whitehouse Station, NJ, USA, 2006; S. 976, ISBN 978-0-911910-00-1.
- M. S. de Winter, C. M. Siegmann and S. A. Szpilfogel, Chem. Ind., 1959, 905 in : Houben-Weyl: Methods of Organic Chemistry Vol IV/16 4. Edition:.Reduktion I , 1980, 668, ISBN 978-3-13-200904-2.
- Europäisches Arzneibuch, 6. Ausgabe, Grundwerk, Deutscher Apotheker-Verlag Stuttgart, 2008.
- H. Lüllmann, K. Mohr, A. Ziegler: Taschenatlas der Pharmakologie, Thieme Verlag 1990, 232–235, ISBN 3-13-707701-X.
- Annetine Gelijns (1991). Innovation in Clinical Practice: The Dynamics of Medical Technology Development. National Academies. S. 167–. NAP:13513.
- Odlind V, Weiner E, Victor A, Johansson ED (1979). Plasma levels of norethindrone after single oral dose administration of norethindrone and lynestrenol. Clin. Endocrinol. (Oxf)., 1979, 10 (1): 29–38. PMID 436304.
