Lunges Reagenz
Lunges Reagenz ist eine nach Georg Lunge benannte Lösung aus Lunge I (Sulfanilsäure) und Lunge II (1-Naphthylamin, auch α-Naphthylamin) und dient in der anorganischen Analytik zum qualitativen und quantitativen Nachweis von Nitrit und Nitrat.[1]
_in_Spalte_1_und_2_und_Natriumnitrid_(NaNO2)_in_Spalte_3_und_Spalte_4_kurz_nach_der_Zugabe.jpg.webp)
_in_Spalte_1_und_2_und_Natriumnitrid_(NaNO2)_in_Spalte_3_und_Spalte_4_nach_dem_Verr%C3%BChren.jpg.webp)
Für den Nachweis von Nitrat muss dieses erst durch Zinkstaub und Eisessig (Ethansäure) zu Nitrit reduziert werden.
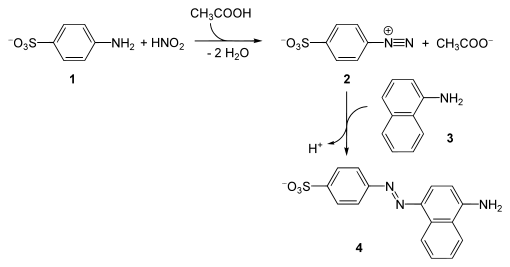
Zur Durchführung des Nachweises wird in ein Reagenzglas etwas Zinkpulver und darüber essigsaure Sulfanilsäure (1) und das α-Naphthylamin (3) gegeben und abgewartet, ob durch Verunreinigungen die Lösung schon vorher rot verfärbt wird. Ist dies nicht der Fall, so kann zum Nachweis ein wenig der zu untersuchenden Substanz (als Lösung oder Feststoff) zugegeben werden.
Um Nitrat auch beim Vorhandensein von Nitrit nachzuweisen, muss man Letzteres vor der Zugabe von Zink mit Amidoschwefelsäure zu Stickstoff reduzieren:
Da die Nachweisreaktion äußerst empfindlich ist, empfiehlt es sich, parallel eine Blindprobe durchzuführen.
Wegen einer vermuteten kanzerogenen Wirkung des in α-Naphthylamin oft enthaltenen β-Naphthylamin[2] wird dieses heutzutage meist durch α-Naphthyl-ethylendiamin (als Dihydrochlorid) ersetzt.
Ein weiterer Nachweis von Nitriten erfolgt mittels Grieß-Reagenz nach Johann Peter Grieß.
Störung
Manche Anionen, wie Bromid (Br−), Iodid (I−), Chlorat (ClO3−), Iodat (IO3−), Sulfid (S2−), Sulfit (SO32−), Thiosulfat (S2O32−), Thiocyanat (SCN−), Chromat (CrO42−), gelbes ([Fe(CN)6]4−) und rotes Blutlaugensalz ([Fe(CN)6]3−) können die Reaktion stören und damit den Nachweis beeinflussen.[3] Br−, I− und S2− können durch Silbersulfat gefällt werden, S2− kann auch mit Cadmiumacetat versetzt werden, so dass Cadmiumsulfid ausfällt. Bei CrO42− wird Bariumchlorid eingesetzt, es fällt dann Bariumchromat aus.[4]
Einzelnachweise
- S. Ebel und H. J. Roth (Herausgeber): Lexikon der Pharmazie, Georg Thieme Verlag, 1987, S. 405, ISBN 3-13-672201-9.
- Eberhard Schweda: Jander/Blasius-Anorganische Chemie I: Theoretische Grundlagen und Qualitative Analyse. 18., völlig neu bearbeitete Auflage. Hirzel Verlag, Stuttgart, ISBN 978-3-7776-2364-1, S. 270.
- Hans P. Latscha, Gerald W. Linti, Helmut A. Klein: Analytische Chemie. Chemie-Basiswissen 3. Springer, Berlin; 4., vollst. überarb. Auflage 2003; ISBN 3-540-40291-8; S. 614.
- Eberhard Gerdes: Qualitative Anorganische Analyse. Vieweg Friedr. + Sohn Ver; 2., korrig. u. überarb. Auflage 2000; ISBN 3-528-16667-3; S. 198.
Literatur
- Joachim Strähle und Eberhard Schweda: Jander/Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie. Hirzel Verlag Stuttgart; 15., überarb. Auflage, ISBN 3-7776-1146-8; S. 614.