Lotaustralin
Lotaustralin ist ein cyanogenes Glycosid, welches in geringer Menge in der namensgebenden Leguminose Lotus australis,[1] in Maniok (Manihot esculenta), in der Limabohne (Phaseolus lunatus)[3], der Rosenwurz (Rhodiola rosea)[4], Weiß-Klee (Trifolium repens)[5] und anderen Pflanzen gefunden wurde.
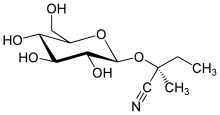
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
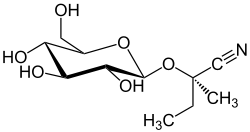 | ||||||||||
| Allgemeines | ||||||||||
| Name | Lotaustralin | |||||||||
| Andere Namen |
(2R)-2-Methyl-2-{[(2S,3R,4S,5S,6R)-3,4,5-trihydroxy-6-(hydroxymethyl)tetrahydro-2H-pyran-2-yl]oxy}butanenitril | |||||||||
| Summenformel | C11H19NO6 | |||||||||
| Kurzbeschreibung |
farblose Nadeln[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 261,27 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
gut löslich in Essigsäureethylester[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Das Epimer (S)-Epilotaustralin kommt vorwiegend in Passionsblumen und dem Zweikorn Triticum dicoccum vor.[6]
Lotaustralin besitzt als Aglycon das Cyanhydrin des Butanons, als Zuckereinheit die β-D-Glucose und ist somit strukturell verwandt mit Linamarin. Die beiden Glycoside unterscheiden sich lediglich durch das jeweilige Aglycon, das sich vom Propanon (Linamarin) bzw. dem Butanon (Lotaustralin) ableitet. In vielen Pflanzen werden auch beide Homologe sowie das Epimere Epilotaustralin gefunden, da die Enzyme der Biosynthese der drei Stoffe dieselben sind. Diese können sowohl Isoleucin zu Lotaustralin oder Epilotaustralin, als auch Valin zu Linamarin umsetzen.[7]
Das Enzym Linamarase kann beide Glycoside spalten, wobei die sehr giftige Blausäure entsteht; deshalb zählt Lotaustralin zu den Cyanogenen Glycosiden. Die Toxizität von Linamarin, Lotaustralin und Epilotaustralin liegen auf ähnlichem Niveau.[6]
Einzelnachweise
- Shmuel Yannai: Dictionary of Food Compounds with CD-ROM: Additives, Flavors, and Ingredients. CRC Press, 2003, ISBN 978-1-58488-416-3, S. 688.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Frehner M, Scalet M, Conn EE: Pattern of the Cyanide-Potential in Developing Fruits : Implications for Plants Accumulating Cyanogenic Monoglucosides (Phaseolus lunatus) or Cyanogenic Diglucosides in Their Seeds (Linum usitatissimum, Prunus amygdalus). In: Plant Physiol. 94, Nr. 1, 1990, S. 28–34. PMID 16667698.
- Akgul Y, Ferreira D, Abourashed E, Khan I: Lotaustralin from Rhodiola rosea roots. In: Fitoterapia. 75, Nr. 6, 2004, S. 612–4. doi:10.1016/j.fitote.2004.06.002. PMID 15351122.
- Notes on poisoning: Trifolium repens. Canadian Poisonous Plants Information System. 30. Mai 2006. Archiviert vom Original am 7. Februar 2012. Abgerufen am 11. Februar 2007.
- J. B. Harborne, H. Baxter, G. P. Moss: Phytochemical dictionary: a handbook of bioactive compounds from plants. 2. Auflage, CRC Press, 1999, ISBN 978-0-7484-0620-3, S. 103.
- J. P. F. D'Mello, C. M. Duffus, J. H. Duffus: Toxic substances in crop plants. Woodhead Publishing, 1991, ISBN 978-0-85186-863-9, S. 208.