Kaliumborhydrid
Kaliumborhydrid ist eine anorganische chemische Verbindung des Borhydride.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
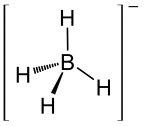 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Kaliumborhydrid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | KBH4 | |||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 53,94 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
1,17 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,494 (20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Gewinnung und Darstellung
Kaliumborhydrid kann durch Reaktion von Natriumborhydrid in Methanol/Wasser mit wässriger Kalilauge gewonnen werden.[4]
Es kann auch durch Reaktion von Diboran mit Kaliumtetramethoxyborhydrid dargestellt werden.[5]
Eigenschaften
Kaliumborhydrid ist ein farbloser Feststoff, der löslich in Wasser ist.[1] Er kristallisiert im Natriumchlorid-Gittertyp mit der Raumgruppe Fm3m (Raumgruppen-Nr. 225). Bei höheren Temperaturen findet eine Umwandlung in eine verwandte tetragonale Struktur statt. Auch bei hohen Drücken findet eine Umwandlung zu einer tetragonalen (4 GPa) mit der Raumgruppe P421c (Raumgruppen-Nr. 114) bzw. orthorhombischen Form (7 GPa) mit der Raumgruppe Pnma (Raumgruppen-Nr. 62) statt.[4][6] Auch bei tiefen Temperaten findet eine Änderung der Kristallstruktur statt. So ändert sich die Kristallstruktur bei 65–70 K in eine tetragonale mit der Raumgruppe P42/nmc (Raumgruppen-Nr. 137).[7]
Verwendung
Kaliumborhydrid wird als spezifisches Reduktionsmittel für Carbonylgruppen von Aldehyden, Ketonen, Säurechloriden und als Schaummittel für Kunststoffe eingesetzt. Es kann auch als Ausgangsstoff zur Herstellung von Chloramphenicol, Vitamin A, Thiopenicol, Atropin und Scopolamin verwendet werden.[1]
Einzelnachweise
- Datenblatt Potassium borohydride, 98% bei AlfaAesar, abgerufen am 2. September 2017 (PDF) (JavaScript erforderlich).
- Egon Wiberg, Nils Wiberg: Inorganic Chemistry. Academic Press, 2001, ISBN 978-0-12-352651-9, S. 951 (eingeschränkte Vorschau in der Google-Buchsuche).
- Datenblatt Kaliumborhydrid (PDF) bei Merck, abgerufen am 2. September 2017.
- Michael Hirscher: Handbook of Hydrogen Storage New Materials for Future Energy Storage. John Wiley & Sons, 2010, ISBN 3-527-62981-5, S. 122 (eingeschränkte Vorschau in der Google-Buchsuche).
- William A. Hart, O. F. Beumel, Thomas P. Whaley: The Chemistry of Lithium, Sodium, Potassium, Rubidium, Cesium and Francium Pergamon Texts in Inorganic Chemistry. Elsevier, 2013, ISBN 978-1-4831-8757-0, S. 399 (eingeschränkte Vorschau in der Google-Buchsuche).
- Ravhi S. Kumar, Eunja Kim, Andrew L. Cornelius: Structural Phase Transitions in the Potential Hydrogen Storage Compound KBH4 under Compression. In: The Journal of Physical Chemistry C. 112, 2008, S. 8452, doi:10.1021/jp0765042.
- Yaroslav Filinchuk, Dmitry Chernyshov, Vladimir Dmitriev: Crystal chemistry of light metal borohydrides. In: Materials Science. 2010, arxiv:1003.5378.


