Jasmonsäure
Jasmonsäure ist ein ubiquitäres Phytohormon und Grundstruktur der Gruppe der Jasmonate, deren Funktion die Regulierung des Wachstums und der Alterung vor allem von Blättern und Wurzeln der Pflanzen ist. Jasmonsäure spielt in einer Vielzahl von Pflanzen eine entscheidende Rolle als Elicitor-Signal bei der Abwehr von biotischem und abiotischem Stress. Wichtigstes Derivat ist ihr Methylester, das Methyljasmonat.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
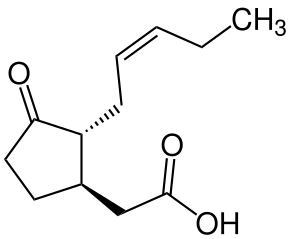 | |||||||||||||
| Struktur von (−)-Jasmonsäure | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Jasmonsäure | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C12H18O3 | ||||||||||||
| Kurzbeschreibung |
viskoses Öl[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 210,27 g·mol−1 | ||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||
| Siedepunkt |
125 °C (0,13 Pa)[1] | ||||||||||||
| Brechungsindex |
1,4885 (bei 19 °C)[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||
Stereochemie
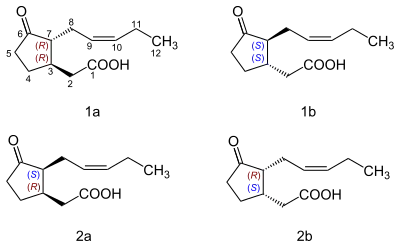
Jasmonsäure ist eine chirale Verbindung, die zwei asymmetrisch substituierte Kohlenstoffatome enthält. Die Verbindung kann daher in vier verschiedenen stereochemischen Formen vorliegen. Die Paare (−)-/(+)-Jasmonsäure (1a/1b) und (+)-epi-/(−)-epi-Jasmonsäure (2a/2b) stellen dabei jeweils spiegelbildliche Moleküle dar, es sind also Enantiomere. Die Paarungen (1a/2a) und (1b/2b) sind Diastereomere.
Natürlich kommt hauptsächlich die (−)-Jasmonsäure und ihr Methylester, (−)-Methyljasmonat, vor.[3]
Biosynthese
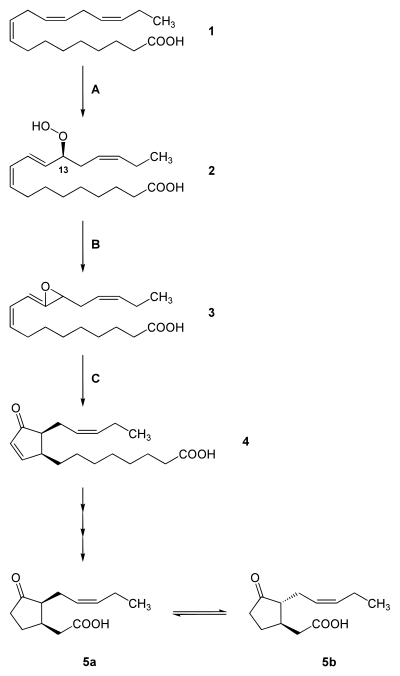
Der Biosyntheseweg von Jasmonaten konnten Brady Vick und Don Zimmerman aufklären.[4][5] So wird Jasmonsäure aus α-Linolensäure gebildet. Die Synthese erfolgt in zwei räumlich getrennten Teilschritten. Der erste Schritt wird von den in der chloroplastidären Membran lokalisierten Enzymen 13-Lipoxygenase (13-LOX), 13-Allenoxidsynthase (13-AOS) und Allenoxidcyclase (AOC) katalysiert. Dabei entsteht das Zwischenprodukt cis-(+)-12-Oxophytodiensäure (OPDA). OPDA oder dessen CoA-Ester wird im zweiten Teilschritt zu den Peroxisomen weitergeleitet. Dort wird der Cyclopentanring von OPDA reduziert. Anschließend katalysieren die Enzyme der β-Oxidation der Fettsäuren auch die Carboxylseitenkette von OPDA und es entsteht (+)-7-iso-Jasmonsäure beziehungsweise das Diastereomer (−)-Jasmonsäure.[6]
Reaktionen
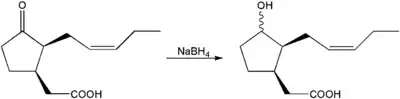
Durch Reduktion, beispielsweise mittels Natriumborhydrid, kann Jasmonsäure zur Synthese von Cucurbinsäure eingesetzt werden.[7] Die Reduktion verläuft nur mit schwacher Diastereoselektivität.
Literatur
- Ushio Sankawa, Derek H. R. Barton, Koji Nakanishi, Otto Meth-Cohn: Comprehensive Natural Products Chemistry: Polyketides and Other Secondary Metabolites Including Fatty Acids and Their Derivatives, ISBN 0-08-043153-4.
- C. Delker, I. Stenzel, B. Hause, O. Miersch, I. Feussner, C. Wasternack: Jasmonate biosynthesis in Arabidopsis thaliana—enzymes, products, regulation. Plant biology (Stuttgart, Germany), 2006 May;8(3):297–306
Einzelnachweise
- Eintrag zu Jasmonsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 7. Mai 2013.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Lalit M. Srivastava: Plant Growth and Development: Hormones and Environment. Academic Press, 2002, ISBN 0-08-051403-0, S. 252 (eingeschränkte Vorschau in der Google-Buchsuche).
- Vick, BA. und Zimmerman, DC. (1984): Biosynthesis of Jasmonic Acid by Several Plant Species. In: Plant Physiol. 75(2); 458–461; PMID 16663643; PDF (freier Volltextzugriff, engl.)
- Vick, BA. und Zimmerman, DC. (1987): Pathways of Fatty Acid Hydroperoxide Metabolism in Spinach Leaf Chloroplasts. In: Plant Physiol. 85(4); 1073–1078; PMID 16665806; PDF (freier Volltextzugriff, engl.)
- Claus Wasternack:Jasmonat – Wirkungsweise, abgerufen am 13. Mai 2013.
- W. Dathe, C. Schindler, G. Schneider, J. Schmidt, A. Porzel, E. Jensen, I. Yamaguchi; Phytochemistry 1991, 30, (6), 1909–1914.