Enterobactin
Enterobactin ist eine chemische Verbindung. Es gehört als Naturstoff zu den Siderophoren (Eisenträger). Vorwiegend gefunden wird es in gramnegativen Bakterien wie Salmonella typhimurium, Escherichia coli und Klebsiella pneumoniae.[1]
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
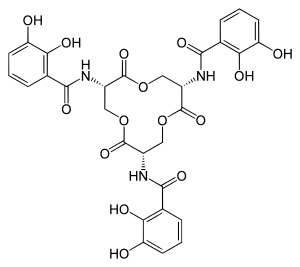 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Enterobactin | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C30H27N3O15 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 669,55 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Biologische Bedeutung
Enterobactin, das ein cyclisches Trimer von N-(2,3-Dihydroxybenzoyl)-L-serin ist, ist in der Lage Eisen koordinativ zu binden. Es bildet mit Eisen-Ionen (Fe3+) außerordentlich stabile Chelatkomplexe. Im Komplex ist das Eisen durch die sechs Sauerstoff-Atome der drei Catechol-Reste oktaedrisch gebunden. Dies führt zu einer sehr hohen Komplexbildungskonstante von K = 1052[1] (zum Vergleich: Die Konstante der Komplexierung von Fe(III) mit EDTA beträgt 1025). Die Affinität zum Fe2+ ist deutlich geringer, eine Reduktion des Zentralatoms bewirkt daher ein Herauslösen des Eisens aus dem Komplex. Diese Eigenschaft wird zum Eisentransport innerhalb der Bakterien verwendet. Enterobactin dient ebenfalls zur Fixierung von Vanadium.[3][4]
In Salmonellen konkurriert das Enterobactin mit den Eisentransportern des Wirtsorganismus.[5]
Biosynthese
Die mehrstufige, enzymatische Biosynthese verläuft über den Shikimisäureweg und geht von Chorisminsäure aus. Diese wird als Chorismat durch Isochorismat-Synthase[6] (eine Mutase) in Isochorismat umgewandelt. Dieses wird durch eine Reihe weiterer Enzyme zum 2,3-Dihydroxybenzoat umgewandelt. Dieses Intermediat wird mit der proteinogenen Aminosäure L-Serin zum N-(2,3-Dihydroxybenzoyl)-L-serin umgesetzt. Dieses wird dimerisiert und bildet das Enterobactin.[7]

Einzelnachweise
- Eintrag zu Enterobactin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. Juni 2014.
- Datenblatt Enterobactin bei Sigma-Aldrich, abgerufen am 25. Juni 2014 (PDF).
- W. Ternes: Biochemie der Elemente: Anorganische Chemie biologischer Prozesse, Springer-Verlag, 2013, ISBN 978-3827430199, S. 75.
- P. Berg, M. Singer: Dealing with Genes: The Language of Heredity, University Science Books, 1. Auflage, 1992, ISBN 978-0935702699, S. 108ff.
- H. Sinell: Einführung in die Lebensmittelhygiene, 4., neu bearbeitete Auflage, Enke Verlag, 2003, ISBN 978-3830440956, S. 22.
- EC 5.4.4.2.
- Daniel L. Purich, R. Donald Allison: The Enzyme Reference, Academic Press, 2003, ISBN 978-0125680417, S. 265 & 486f.