Dinitrobenzole
Die Dinitrobenzole (nach der IUPAC-Nomenklatur Dinitrobenzen, auch DNB) bestehen aus einem Benzolring mit zwei Nitrogruppen (–NO2) als Substituenten. Durch unterschiedliche Anordnung der Nitrogruppen ergeben sich drei Konstitutionsisomere mit der Summenformel C6H4N2O4. Das m-Dinitrobenzol fällt u. a. bei der Sprengstoffherstellung an.
Vertreter
| Dinitrobenzole | ||||||
| Name | o-Dinitrobenzol | m-Dinitrobenzol | p-Dinitrobenzol | |||
| Andere Namen | 1,2-Dinitrobenzol | 1,3-Dinitrobenzol | 1,4-Dinitrobenzol | |||
| Strukturformel | 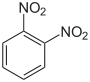 |
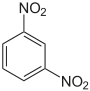 |
||||
| CAS-Nummer | 528-29-0 | 99-65-0 | 100-25-4 | |||
| 25154-54-5 (Isomerengemisch)[1] | ||||||
| PubChem | 10707 | 7452 | 7492 | |||
| Summenformel | C6H4N2O4 | |||||
| Molare Masse | 168,11 g·mol−1 | |||||
| Aggregatzustand | fest | |||||
| Kurzbeschreibung | farblose Kristalle | gelbliche Kristalle | farblose Kristalle | |||
| Schmelzpunkt | 118 °C[2] | 89 °C[3] | 174 °C[4] | |||
| Siedepunkt | 318 °C[2] | 291 °C[3] | 299 °C[4] | |||
| Dichte | 1,565 (17 °C)[5] | 1,575 (18 °C)[5] | 1,625 (18 °C)[5] | |||
| Dampfdruck | 0,08 Pa (30 °C)[6] | 0,07 Pa (30 °C)[6] | ||||
| 0,34 Pa (50 °C)[6] | 0,23 Pa (50 °C)[6] | |||||
| Löslichkeit | unlöslich in Wasser | |||||
| GHS- Kennzeichnung |
aus Verordnung (EG) Nr. 1272/2008 (CLP),[7] ggf. erweitert
| |||||
| H- und P-Sätze | 300+310+330‐373‐410[2] | 330‐310‐300‐373‐410[3] | 300‐310‐330‐373‐410[4] | |||
| keine EUH-Sätze | ||||||
| 260‐280‐284‐301+310+330‐302+352+310‐361+364‐304+340+310[2] | 260‐264‐273‐280‐284‐301+310[3] | 260‐264‐273‐280‐284‐301+310[4] | ||||
| MAK-Wert | Schweiz: 0,15 ml·m−3 bzw. 1 mg·m−3[8] | |||||
Eigenschaften
Die Dinitrobenzole sind allesamt kristalline Feststoffe. Die Siedepunkte der drei Isomere liegen relativ nah beieinander, während sich ihre Schmelzpunkte deutlicher unterscheiden. Das p-Dinitrobenzol, das die höchste Symmetrie aufweist, besitzt den höchsten Schmelzpunkt.
Darstellung
Das m-Dinitrobenzol ist durch erneute Nitrierung von Nitrobenzol zugänglich, die Reaktion läuft mit Schwefelsäure säurekatalysiert ab. Der −I-Effekt und der −M-Effekt der Nitrogruppe des Nitrobenzols bewirken zu 93 % eine Direktion in die meta-Stellung. Die ortho- und para-Produkte treten nur zu 6 bzw. 1 % auf.[9]

Verwendung
Eine Reduktion des m-Dinitrobenzols mit Natriumsulfid in wässriger Lösung führt zu m-Nitroanilin, die komplette Reduktion (Fe/HCl) zu m-Phenylendiamin.[10]
Weblinks
Einzelnachweise
- Eintrag zu Dinitrobenzol, Isomere in der GESTIS-Stoffdatenbank des IFA, abgerufen am 12. März 2017. (JavaScript erforderlich)
- Eintrag zu 1,2-Dinitrobenzol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 4. März 2020. (JavaScript erforderlich)
- Eintrag zu 1,3-Dinitrobenzol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 4. März 2020. (JavaScript erforderlich)
- Eintrag zu 1,4-Dinitrobenzol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 4. März 2020. (JavaScript erforderlich)
- Brockhaus ABC Chemie, VEB F.A. Brockhaus Verlag, Leipzig 1971.
- H: Félix-Rivera, M.L. Ramírez-Cedeño, R.A. Sánchez-Cuprill, S.P. Hernández-Rivera: Triacetone triperoxide thermogravimetric study of vapor pressure and enthalpy of sublimation in 303–338 K temperature range; in: Thermochim. Acta, 2011, 514, S. 37–43 (doi:10.1016/j.tca.2010.11.034).
- Eintrag zu Dinitrobenzene im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 11. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach Dinitrobenzol (alle Isomeren)), abgerufen am 4. März 2020.
- Joachim Buddrus: Grundlagen der organischen Chemie, 3. Auflage, de Gruyter, Berlin 2003, ISBN 3-11-014683-5, S. 360.
- Beyer / Walter: Lehrbuch der Organischen Chemie, 19. Auflage, S. Hirzel Verlag, Stuttgart 1981, ISBN 3-7776-0356-2, S. 536, 542.


