Defibrotid
Defibrotid, vertrieben unter dem Markennamen Defitelio, ist eine Mischung aus einzelsträngigen Oligonukleotiden, die aus der Darmschleimhaut von Schweinen extrahiert wird. Es wird zur Behandlung der venösen okklusiven Leberkrankheit bei Menschen eingesetzt, die eine Knochenmarktransplantation hatten.[1][2][3]
| Nukleinsäure | |
|---|---|
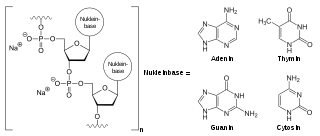 | |
| Defibrotid-Natriumsalz (n = 2–50) | |
| Allgemeines | |
| Freiname | Defibrotid |
| Andere Namen |
JZP-381 |
| Identifikatoren | |
| CAS-Nummer | |
| Wirkstoffdaten | |
| DrugBank | |
| ATC-Code |
B01AX01 |
| Wirkstoffgruppe | |
| Wirkmechanismus |
Fibrinolytisch, Thrombozytenfunktions-hemmend |
| Eigenschaften | |
| Größe |
|
Zulassung
Defibrotid wurde im Oktober 2013 in der Europäischen Union,[3] im März 2016 in den Vereinigten Staaten[4] und im Juli 2020 in Australien[5] für die medizinische Verwendung zugelassen. Defibrotid ist die erste von der FDA zugelassene Therapie zur Behandlung von schwerer hepatischer Lebervenenverschlusskrankheit, einer seltenen und lebensbedrohlichen Lebererkrankung.[5]
Eigenschaften
Defibrotid ist eine Mischung von Oligonukleotiden, die durch chemische Spaltung (Depolymerisation) aus Schweine-DNA gewonnen wird. Die Substanz ist überwiegend einzelsträngig, wobei die Stränge unterschiedliche Basensequenzen, Längen und Sekundärstrukturen aufweisen; entfaltet, gefaltet oder kombiniert. Die mittlere Stranglänge beträgt 50 Basen, bei einer mittleren molaren Masse von 17 ± 4 kDa.
Defibrotid ist stark heterogen aufgebaut und neben der durchschnittlichen Stranglänge charakterisiert durch den Anteil einer jeden Nukleobase und den Anteil an doppelsträngigen Strukturen.[6] Die Oligonukleotide liegen als Natriumsalz vor.
Pharmakologie
Der Wirkmechanismus von Defibrotid ist nur unzureichend bekannt. In-vitro-Studien haben gezeigt, dass es das Endothel, das die Blutgefäße auskleidet, vor Schäden durch Fludarabin, ein Chemotherapeutikum, und vor einigen anderen Erkrankungen wie Serum-Mangel schützt. Es scheint auch die t-PA-Funktion zu erhöhen und die Plasminogen-Aktivator-Inhibitor-1-Aktivität zu verringern.[2][1]
Anwendungen
In der Europäischen Union ist Defibrotid für die Behandlung der schweren hepatischen veno-okklusiven Erkrankung (VOD), auch bekannt als sinusoidales obstruktives Syndrom (SOS), im Rahmen einer hämatopoetischen Stammzelltransplantation (HSCT) bei Erwachsenen, Jugendlichen, Kindern und Säuglingen ab einem Monat indiziert.[3]
Defibrotid wird zur Behandlung der veno-okklusiven Erkrankung der Leber von Menschen nach einer Knochenmarktransplantation eingesetzt, mit unterschiedlichen Einschränkungen in den USA und der Europäischen Union.[1] Bis 2016 wurden jedoch keine randomisierten placebokontrollierten Studien durchgeführt.[7]
Die Gabe erfolgt als intravenöse Infusion.
Die hämatopoetische Stammzelltransplantation (HSCT) ist ein Verfahren, das bei einigen Menschen durchgeführt wird, um bestimmte Blut- oder Knochenmarkskrebsarten zu behandeln.[8] Unmittelbar vor einer HSCT-Prozedur erhält ein Patient eine Chemotherapie.
Kontraindikationen und Vorsichtsmaßnahmen
Die Anwendung von Defibrotid bei Menschen, die bereits Antikoagulanzien einnehmen, ist gefährlich und die Anwendung anderer Medikamente, die die Thrombozytenaggregation beeinflussen, wie NSAIDs, sollte mit Vorsicht erfolgen. Defibrotid sollte nicht an Menschen verabreicht werden, die Schwierigkeiten haben, einen stabilen Blutdruck zu halten.[2] Schwangere Frauen sollten Defibrotid nicht einnehmen und sollten nicht schwanger werden, während sie es einnehmen; es wurde nicht an schwangeren Frauen getestet, aber in normalen Dosen verursachte es einen hämolytischen Abort bei Ratten.[2]
Nebenwirkungen
Zu den häufigsten Nebenwirkungen gehören niedriger Blutdruck (Hypotonie), Durchfall, Erbrechen, Übelkeit und Nasenbluten (Epistaxis). Zu den schwerwiegenden potenziellen Nebenwirkungen, die identifiziert wurden, gehören Blutungen (Hämorrhagie) und allergische Reaktionen. Defibrotid sollte nicht bei Menschen angewendet werden, die Hämophilie haben oder die Gerinnungshemmer oder andere Medikamente einnehmen, die die Fähigkeit des Körpers zur Bildung von Blutgerinnseln herabsetzen.[8][3] Die Anwendung des Medikaments ist im Allgemeinen durch ein starkes Risiko von lebensbedrohlichen Blutungen im Gehirn, den Augen, der Lunge, dem Magen-Darm-Trakt, den Harnwegen und der Nase eingeschränkt. Bei manchen Menschen treten Überempfindlichkeitsreaktionen auf.[2]
Weblinks
- Defitelio auf der Website der europäischen Arzneimittelagentur
Einzelnachweise
- DailyMed - DEFITELIO- defibrotide sodium injection, solution. Abgerufen am 31. März 2021.
- Defitelio 80 mg/mL concentrate for solution for infusion - Summary of Product Characteristics (SmPC) - (emc). Abgerufen am 31. März 2021.
- Defitelio. Abgerufen am 31. März 2021 (englisch).
- Defitelio Injection. Abgerufen am 31. März 2021.
- Australian Government Department of Health Therapeutic Goods Administration: Defitelio. 31. Juli 2020, abgerufen am 31. März 2021 (englisch).
- Defitelio, Assessment report, EMA, 25. Juli 2013.
- Jean-Hugues Dalle, Sergio A. Giralt: Hepatic Veno-Occlusive Disease after Hematopoietic Stem Cell Transplantation: Risk Factors and Stratification, Prophylaxis, and Treatment. In: Biology of Blood and Marrow Transplantation: Journal of the American Society for Blood and Marrow Transplantation. Band 22, Nr. 3, März 2016, S. 400–409, doi:10.1016/j.bbmt.2015.09.024, PMID 26431626.
- Office of the Commissioner: FDA approves first treatment for rare disease in patients who receive stem cell transplant from blood or bone marrow. 24. März 2020, abgerufen am 31. März 2021 (englisch).