Chrom(III)-sulfat
Chrom(III)-sulfat (Cr2(SO4)3) ist ein Salz der Schwefelsäure.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
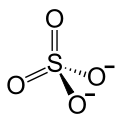 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Chrom(III)-sulfat | ||||||||||||||||||
| Andere Namen |
Chromsulfat | ||||||||||||||||||
| Summenformel |
| ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | |||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
3,01 g·cm−3 (Anhydrat bei 20 °C)[3] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
schlecht in Wasser[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
Chrom(III)-sulfat kann durch die Reduktion von Dichromaten dargestellt werden:
Durch Reaktion von Kaliumdichromat, Schwefelsäure und Schwefelwasserstoff kann Chrom(III)-sulfat hergestellt werden. Als Nebenprodukte entstehen Kaliumsulfat und Wasser:
Alternativ ist zum Beispiel auch der Einsatz von Ethanol statt Schwefelwasserstoff möglich, wobei – neben dem Chrom(III)-sulfat – Kaliumsulfat, Essigsäure und Wasser entstehen:
Über diese Reaktionen erhält man allerdings kristallwasserhaltiges Chrom(III)-sulfat. Das Anhydrat lässt sich durch Entfernen des Kristallwassers bei 280 °C im CO2-Strom darstellen.[6]
Eigenschaften
_sulfate.jpg.webp)
-sulfatl%C3%B6sung.jpg.webp)
Wasserfrei bildet Chrom(III)-sulfat rot-braune, hexagonale Kristalle;[1] mit Kristallwasser als Pentahydrat (Cr2(SO4)3 · 5 H2O) ist es dunkelgrün. Das Dodecahydrat und das Octadecahydrat sind hingegen lila bis violett.[2]
Absolut wasserfreies Chrom(III)-sulfat ist in Wasser unlöslich[6], die kristallwasserhaltigen Formen sind hingegen unter Bildung von blau bis violett gefärbten Aquakomplexen wasserlöslich, die beim Erhitzen in grün gefärbte Sulfatokomplexe übergehen.[7]
Das Pentahydrat hat eine trikline Kristallstruktur, isotyp zu der von Kupfersulfat-Pentahydrat.[8]
Verwendung
Chrom(III)-sulfat wird als Textilbeize oder zur Gerbung von Leder verwendet. Es wird zudem als Ausgangsstoff für andere Chromverbindungen benutzt.[3][2]
Einzelnachweise
- SLAC: PHYSICAL CONSTANTS OF INORGANIC COMPOUNDS (PDF; 391 kB).
- Eintrag zu Chrom(III)-sulfat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 20. Juni 2014.
- Eintrag zu Chrom(III)-sulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 4. September 2016. (JavaScript erforderlich)
- jtbaker.com: Chromium Sulfate.
- Datenblatt Chromium(III) sulfate hydrate, Reagent Grade bei AlfaAesar, abgerufen am 7. Dezember 2019 (PDF) (JavaScript erforderlich).
- Gmelins Handbuch der anorganischen Chemie - Nr. 52 Chrom, Die Verbindungen (ohne Komplexbindungen mit neutralen Liganden), 8. Auflage Berlin, 1962.
- Jander-Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie, 5. Auflage, S. Hirzel, Stuttgart-Leipzig 1965, S. 225
- Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1509.
