Chlorsulfonylisocyanat
Chlorsulfonylisocyanat ist eine chemische Verbindung aus der Gruppe der Isocyanate. Sie wurde 1952 zuerst von Roderich Graf synthetisiert und 1956 veröffentlicht.[5][6]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
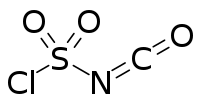 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Chlorsulfonylisocyanat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | ClSO2NCO | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit stechendem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 141,53 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
1,63 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
106 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,447 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Gewinnung und Darstellung
Chlorsulfonylisocyanat kann durch Reaktion von Chlorcyan mit Schwefeltrioxid gewonnen werden.[7][8]
Eigenschaften
Chlorsulfonylisocyanat ist eine brennbare, schwer entzündbare, leicht flüchtige, an Luft rauchende, farblose Flüssigkeit mit stechendem Geruch, die sich in Wasser und Ethanol mit heftiger bis explosionsartiger Reaktion zersetzt. Sie zersetzt sich bei Temperaturen über 300 °C. Die Verbindung ist das reaktivste bekannte Isocyanat.[1][2] Der Winkel zwischen Cl-S und N=C beträgt 94° und die NCO-Gruppe ist nicht linear.[9]
Verwendung
Chlorsulfonylisocyanat wird zur Herstellung anderer chemischer Verbindungen verwendet. Es überführt Amine, Alkohole und Säuren in N-Chlorsulfonylharnstoffe, -urethane usw.[2]
Einzelnachweise
- Eintrag zu Chlorsulfonylisocyanat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Eintrag zu N-Carbonylsulfamoylchlorid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 18. November 2016.
- Datenblatt Chlorosulfonyl isocyanate, Lonza quality, 99.0-100.3% (w/w) (T) bei Sigma-Aldrich, abgerufen am 18. November 2016 (PDF).
- Datenblatt Chlorsulfonylisocyanat (PDF) bei Merck, abgerufen am 18. November 2016.
- Jerald K. Rasmussen, Alfred Hassner: Recent developments in the synthetic uses of chlorosulfonyl isocyanate. In: Chemical Reviews. 76, 1976, S. 389, doi:10.1021/cr60301a004.
- Roderich Graf: Über die Umsetzung von Chlorcyan mit Schwefeltrioxyd. In: Chemische Berichte. 89, 1956, S. 1071, doi:10.1002/cber.19560890437.
- R. Graf: Chlorosulfonyl Isocyanate In: Organic Syntheses. 46, 1966, S. 23, doi:10.15227/orgsyn.046.0023; Coll. Vol. 5, 1973, S. 226 (PDF).
- Google Patente: Patent EP0294613A1 - Verfahren und Anlage zur kontinuierlichen Herstellung von Chlorsulfonylisocyanat, abgerufen am 18. November 2016.
- Durga Nath Dhar, Preeti Dhar: The Chemistry of Chlorosulfonyl Isocyanate. World Scientific, 2002, ISBN 978-981-238-081-4, S. 1 (eingeschränkte Vorschau in der Google-Buchsuche).


