Calciumoxalat
Calciumoxalat ist ein Calciumsalz der Oxalsäure. Es besitzt die Summenformel CaC2O4 und gehört zur Stoffgruppe der Oxalate.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
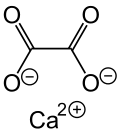 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Calciumoxalat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | CaC2O4 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Kristalle (Monohydrat)[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 128,10 g·mol−1 146,12 g·mol−1 (Monohydrat) | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser[1] (0,0061 g·l−1 bei 20 °C)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−1360,6 kJ/mol[7] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Vorkommen


In der Natur kommt Calciumoxalat als Hauptbestandteil von Nierensteinen und Bierstein vor. Darüber hinaus kommt es in vielen Pflanzen als Fraßverteidigung vor (so z. B. in der Schild-Ampfer, Schmerwurz, Pastinaken, Taro und in Dieffenbachien und anderen Aronstabgewächsen). Auch im Gewebe von Kakteen sammelt sich Calciumoxalat. So besteht 85 % der Trockenmasse in Cephalocereus senilis aus Calciumoxalat. Die Kristallform des Calciumoxalats in den Pflanzenzellen ist meistens prismatisch mit spitzen Winkeln oder sternförmig (Drusen). Seltener zeigt sich ein nadeliger Kristallhabitus.[8] Bündel aus nadelförmigen Calciumoxalat-Kristallen werden in der Botanik als Raphiden bezeichnet (nach griech. rhaphis: Nadel), sie kommen nur in einigen systematischen Gruppen vor und haben dadurch diagnostischen Wert in der Systematik.[9] Neben diesen biologischen Quellen kommt Calciumoxalat in der Natur in Hydratform als die seltenen Mineralien Whewellit und Weddellit vor. Das Mineral des Trihydrats heißt Caoxit.
Gewinnung und Darstellung
Calciumoxalat ist ein Zwischenprodukt bei der Herstellung von Oxalsäure. Dabei wird Natriumoxalat mit Calciumhydroxid in das schwerlösliche Calciumoxalat überführt, aus dem die Oxalsäure mit Schwefelsäure freigesetzt wird.
Kristallstrukturen
Wasserfreies Calciumoxalat existiert nicht als Einkristall, sondern wird durch Erhitzen aus den Hydraten gewonnen. Dessen Kristallstruktur wurde deshalb durch Röntgenbeugung am kristallinen Pulver bestimmt und zeigt monokline Symmetrie mit der Raumgruppe P2/m (Raumgruppen-Nr. 10).[10] Calciumoxalat-Monohydrat kristallisiert ebenfalls im monoklinen Kristallsystem. Bei Raumtemperatur ist die Raumgruppe P21/n (Nr. 14, Stellung 2) und oberhalb von 328 K wird die Raumgruppe zu I2/m (Nr. 12, Stellung 3).[11][12] Calciumoxalat-Dihydrat kristallisiert im tetragonalen Kristallsystem mit der Raumgruppe I4/m (Nr. 87).[13] Calciumoxalat-Trihydrat kristallisiert im triklinen Kristallsystem mit der Raumgruppe P1 (Nr. 2).[14]
Chemische Eigenschaften
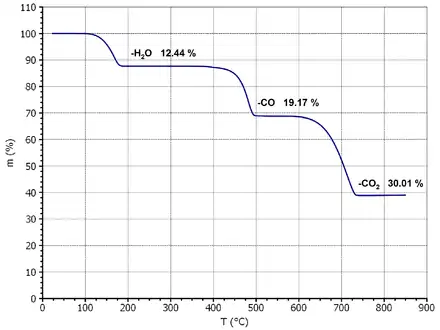
Calciumoxalat ist ein farbloses Salz der Oxalsäure. Die Verbindung bildet ein stabiles Monohydrat. Beim Erhitzen wird ab 110 °C zunächst das Kristallwasser abgegeben. Oberhalb von 300 °C zerfällt die Verbindung unter Freisetzung von Kohlenmonoxid und der Bildung von Calciumcarbonat. Dieses zersetzt sich beim weiteren Erhitzen oberhalb von 500 °C in Calciumoxid und Kohlendioxid.[15][16][17][18]
Alle drei Reaktionschritte verlaufen endotherm.[18] In Gegenwart von Luftsauerstoff erfolgt die zweite Reaktionsstufe als exotherme Oxidationsreaktion unter der Bildung von Kohlendioxid.[18]
Mit einem Dihydrat und einem Trihydrat sind noch zwei weitere, metastabile Hydrate bekannt.[16]
Verwendung
Calciumoxalat dient als Nachweis für Calciumionen. Gibt man eine oxalathaltige Lösung zur zu bestimmenden calciumhaltigen Lösung, fällt das schwer lösliche Calciumoxalat aus. Weiterhin dient es als Bleichmittel und findet als Metallreiniger Verwendung. Es wird auch als Glanzschicht auf der Oberfläche von Natursteinen erzeugt (siehe Glanz von Natursteinen).
Calciumoxalat-Monohydrat wird in der Thermogravimetrie zur Kalibrierung von Thermowaagen verwendet.
Einzelnachweise
- Eintrag zu Calciumoxalat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. September 2014.
- Datenblatt Calciumoxalat-Monohydrat bei AlfaAesar, abgerufen am 31. Januar 2010 (PDF) (JavaScript erforderlich).
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 85. Auflage. (Internet-Version: 2005), CRC Press/Taylor and Francis, Boca Raton, FL, PHYSICAL CONSTANTS OF INORGANIC COMPOUNDS, S. 4-49 – 4-49.
- Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag salts of oxalic acid with the exception of those specified elsewhere in this Annex im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Datenblatt Calciumoxalat bei Sigma-Aldrich, abgerufen am 30. November 2021 (PDF).
- Datenblatt Calciumoxalat (PDF) bei Carl Roth, abgerufen am 31. Januar 2010.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-20.
- T. Terrazas Salgado, J. Mauseth: Cacti: Biology and uses. Hrsg.: P. S. Nobel. University of California Press, Berkeley 2002, ISBN 0-520-23157-0, Shoot anatomy and morphology, S. 23–40 (Volltext in der Google-Buchsuche [abgerufen am 12. Juni 2016]).
- Gerhard Wagenitz: Wörterbuch der Botanik. 2. Auflage, Spektrum Verlag, Heidelberg und Berlin 2003. ISBN 978-3-937872-94-0, auf S. 272.
- O. Hochrein, A. Thomas, R. Kniep: Revealing the Crystal Structure of Anhydrous Calcium Oxalate, Ca[C2O4], by a Combination of Atomistic Simulation and Rietveld Refinement. In: Zeitschrift für anorganische und allgemeine Chemie. Band 634, Nr. 11, 2008, S. 1826–1829, doi:10.1002/zaac.200800207.
- S. Deganello: The basic and derivative structures of calcium oxalate monohydrate. In: Zeitschrift für Kristallographie. Band 152, Nr. 1-4, 1980, S. 247–252, doi:10.1524/zkri.1980.152.14.247.
- S. Deganello: The structure of whewellite at 328 K. In: Acta Crystallographica Section B. Band 37, Nr. 4, 1981, S. 826–829, doi:10.1107/S056774088100441X.
- C. Sterling: Crystal structure analysis of weddellite. In: Acta Crystallographica. Band 18, Nr. 5, 1965, S. 917–921, doi:10.1107/S0365110X65002219.
- S. Deganello, A. R. Kampf, P. B. Moore: The crystal structure of calcium oxalate trihydrate. In: American Mineralogist. Band 66, Nr. 7-8, 1981, S. 859–865.
- N. Kutaish, P. Aggarwal, D. Dollimore: Thermal analysis of calcium oxalate samples obtained by various preparative routes. In: Thermochim. Acta. 297, 1997, S. 131–137. doi:10.1016/S0040-6031(97)00002-6.
- G. Sadovska, G. Wolf: Enthalpy of dissolution and thermal dehydration of calcium oxalate hydrates. In: J. Therm. Anal. Calorim. 119, 2015, S. 2063–2068. doi:10.1007/s10973-014-4350-x.
- H. L. Anderson, A. Kemmler, G. W. H. Höhne, K. Heldt, R. Strey: Round robin test on the kinetic evaluation of a complex solid state reaction from 13 European laboratories. Part 1. Kinetic TG-analysis. In: Thermochim. Acta. 332, 1999, S. 33–53. doi:10.1016/S0040-6031(99)00045-3.
- H. L. Anderson, R. Strey, G. W. H. Höhne, A. Kemmler, K. Heldt: Round robin test on the kinetic evaluation of a complex solid state reaction from 13 European laboratories. Part 2. Kinetic DSC-analysis. In: Thermochim. Acta. 332, 1999, S. 55–70. doi:10.1016/S0040-6031(99)00046-5.
