Arsensulfide
Arsensulfide sind Sulfid-Verbindungen der chemischen Elemente Arsen und Schwefel in der Form AsxSy.
Ausbildungsformen
Es sind verschiedene Arsensulfide bekannt, von denen mehrere in der Natur vorkommen:
- Tetraarsensulfid As4S, als Mineral Duranosit
- Tetraarsentrisulfid As4S3, in der Natur als Mineral Dimorphin zu finden.
- Arsen(II)-sulfid, Tetraarsentetrasulfid, As4S4, auch Arsendisulfid As2S2, in der Verhältnisformel auch mit AsS angegeben
- Ist in der Natur als Mineral Realgar (α-As4S4), Bonazziit (β-As4S4) und Pararealgar (γ-As4S4) bekannt. Es bildet Kristalle, von roter Farbe (in der α-Struktur, Rauschrot) bis orangegelb (γ-Struktur)
- Arsen(III)-sulfid, Tetraarsenhexasulfid As4S6 bzw. Arsentrisulfid As2S3
- Es bildet orange- bis hochgelbe Kristalle (Rauschgelb) und entsteht in der Natur in Form der Minerale Auripigment und Anauripigment. Als Pigment Auripigment ausschließlich in rein goldgelber Form (Königsgelb).
- Arsen(V)-sulfid, Arsenpentasulfid As2S5 kommt in der Natur nicht vor. Es ist ein zitronengelbes Pulver.
- Tetraarsenpentasulfid As4S5, als Mineral Uzonit
- As8S9, als Mineral Alacránit
Struktur
Arsensulfide haben allgemein die Summenformel As2Sn, bilden aber meist komplizierte Käfigstrukturen der Form As4Sn. Arsen ist dabei dreibindig, geht also eine Bindung mit je drei weiteren Atomen (Schwefel oder Arsen) ein. Schwefel ist zweibindig und steht brückenbildend zwischen je zwei Arsenatomen.
Arsenpentasulfid bildet die Ausnahme, da in dieser Verbindung an jedem Arsen-Atom zusätzlich noch je eine Doppelbindung zu Schwefel vorhanden ist.
Im Festkörper liegt Arsen(III)-sulfid als As2S3 in einer polymeren Struktur vor, die Käfigstruktur (hier:Adamantan-Struktur) bildet sich erst in der Gasphase.
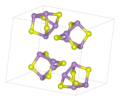 As4S4 (Realgar)
As4S4 (Realgar)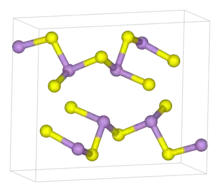 As2S3 (Orpiment) im Festkörper
As2S3 (Orpiment) im Festkörper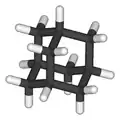 Adamantan-Struktur
Adamantan-Struktur
Eigenschaften
Arsensulfide sind im Allgemeinen schwer wasserlöslich und daher in reinem Zustand nicht giftig.
- an der Luft bildet sich aber meist eine geringe Menge des Arsen(III)-oxid (Arsenik).
- As2S3 (Auripigment) ist nicht löslich in Wasser und Säuren, wird also im Magen von der Salzsäure nicht abgebaut. As4S4 (Realgar) ist aber alkalisch löslich und bildet mit Säuren sowie beide mit Kalilauge giftige Dämpfe.
- die Arsensulfide reagieren bei Verbrennung zu Arsen(III)-oxid und Schwefel bzw. Schwefeldioxid
- sowohl reines Arsen wie auch Arsen(III)-oxid als Arsenolith treten in gelben Modifikationen auf. Diese können in natürlichen Vorkommen wie auch synthetischen Produkten vorliegen
Arsentrioxid ist eines der giftigsten Mineralien und krebserregend und für viele Lebewesen schädlich. Die oral aufgenommene, tödliche Dosis kann für den Menschen bereits bei weniger als 0,1 g liegen. Aus diesen Gründen gelten alle Arsensulfide prinzipiell als hochgiftig und umweltschädlich und unterliegen strengsten Sicherheitsbestimmungen.
| Arsensulfide | |||||||||
| Name | Arsen(II)-sulfid | Arsen(III)-sulfid | Arsen(V)-sulfid | ||||||
| Andere Namen | |||||||||
| Natürliches Vorkommen | Realgar | Auripigment | |||||||
| Summenformel | As4S4 | As2S3 | As2S5 | ||||||
| CAS-Nummer | 12044-79-0 | 1303-33-9 | 1303-34-0 | ||||||
| PubChem | 139298 | 71586773 | 3371533 | ||||||
| Molare Masse | 427,92 g·mol−1 | 246,04 g·mol−1 | 310,14 g·mol−1 | ||||||
| Aggregatzustand | fest[1] | fest[2] | |||||||
| Kurzbeschreibung | Stücke oder kristallines Pulver goldgelb, geruchlos[1] |
||||||||
| Schmelzpunkt | 300…325 °C[1] | >300 °C[2] | |||||||
| Dichte | 3,46 g·cm−3[1] | ||||||||
| Löslichkeit in Wasser | 0,51 mg·l−1 bei 18 °C[1] | ||||||||
| GHS- Kennzeichnung |
aus Verordnung (EG) Nr. 1272/2008 (CLP),[3] ggf. erweitert
|
aus Verordnung (EG) Nr. 1272/2008 (CLP),[4] ggf. erweitert
|
aus Verordnung (EG) Nr. 1272/2008 (CLP),[5] ggf. erweitert
| ||||||
| H- und P-Sätze | 301‐331‐410 | 301‐331‐410 | 301‐331‐410 | ||||||
| ? | 270‐273‐302+352‐309+310‐501[1] | 261‐273‐301+310+330‐304+340+312‐391‐403+233[2] | |||||||
Künstliche Herstellung
Die meisten Arsensulfide können durch Zusammenschmelzen von Arsen und Schwefel im entsprechenden Mengenverhältnis gewonnen werden. Arsen(V)-sulfid entsteht aus Arsensäure und Schwefelwasserstoff.[6]
Literatur
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 91.–100., verbesserte und stark erweiterte Auflage. Walter de Gruyter, Berlin 1985, ISBN 3-11-007511-3.
- Stefan Weiß: Das große Lapis Mineralienverzeichnis. Alle Mineralien von A – Z und ihre Eigenschaften. Stand 03/2018. 7., vollkommen neu bearbeitete und ergänzte Auflage. Weise, München 2018, ISBN 978-3-921656-83-9.
Weblinks
- Arsensulfide. In: Meyers Konversations-Lexikon. 4. Auflage. Band 1, Verlag des Bibliographischen Instituts, Leipzig/Wien 1885–1892, S. 875.
- Eintrag zu Arsensulfide. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. November 2020.
- Arsensulfide. Spektrum.de, abgerufen am 10. November 2020.
Einzelnachweise
- Eintrag zu CAS-Nr. 1303-33-9 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 27. Januar 2017. (JavaScript erforderlich)
- Datenblatt Arsenic(V) sulfide bei Sigma-Aldrich, abgerufen am 27. Januar 2017 (PDF).
- Eintrag zu Arsen(II)-sulfid im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 27. Januar 2017. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Arsenverbindungen, mit Ausnahme der namentlich in diesem Anhang bezeichneten im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 27. Januar 2017. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Arsen(V)-sulfid im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 27. Januar 2017. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 603.

