Arenoxide
Arenoxide sind chemische Verbindungen, bei denen eine der „Doppelbindungen“ eines aromatischen Ringsystems in ein Epoxid umgewandelt wurde. Das einfachste Arenoxid ist Benzoloxid.[1]
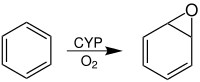
Diese Umwandlung geschieht unter der katalytischen Wirkung eines Enzyms im Körper, wenn fremde aromatische Substanzen, wie z. B. Benzol, in diesen gelangen. Dies geschieht, um eine wasserlösliche Verbindung zu schaffen, welche schließlich über die Niere ausgeschieden werden kann (Biotransformation). Das Enzym, welches aromatische Kohlenwasserstoffe in Arenoxide umwandelt und somit entgiftend wirkt, gehört zu den Cytochrom P450-Enzymen (auch CYP).[1] Ein Arenoxid kann sich entweder wie ein Epoxid verhalten und bei Angriff durch ein Nucleophil ein Additionsprodukt bilden, oder es lagert sich zu einem Phenol um.
Reaktionen
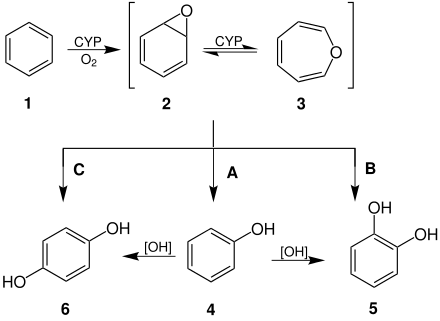
Benzol (1) wird im Körper oxidiert (P-450), es entsteht das Oxiran 2. Benzoloxid (2) und Oxepin (3) liegen im chemischen Gleichgewicht etwa im Verhältnis 1:1 vor. Das Gleichgewicht zwischen 2 und 3 ist ein Valenztautomerie-Gleichgewicht.[2]
- 2 bzw. 3 reagiert zu einem Hydrochinon (6) (Schritt C) und kann zu einem Chinon weiteroxidiert werden (Polyphenoloxidase: Reaktionsmechanismus siehe Chinone).
- Durch die Hydrolyse der Epoxid-Gruppe – durch eine Epoxid-Hydrolase (B) (siehe Benzo[a]pyren) – entsteht Brenzcatechin, das zu Benzochinon (5) weiteroxidiert werden kann.
- Dieses lagert sich zu Phenol (4) um: Arenoxidumlagerung (A)[3]
Mechanismus der Arenoxidumlagerung

Der dreigliedrige Ring des Benzoloxides (1) nimmt ein Proton eines Protonendonators auf. Je stabiler das gebildete Carbokation (2), desto leichter öffnet sich der Ring. Durch eine 1,2-Hydridverschiebung bildet sich ein Enon (3). Die Abgabe eines Protons in die Lösung führt unter Rearomatisierung zur Bildung des Phenols (4).
Einzelnachweise
- Paula Yurkanis Bruice: Organische Chemie, Pearson Education Inc., 2011, 5. Auflage, S. 421, ISBN 978-3-8273-7190-4.
- E. Vogel, H. Günther: Benzoloxid-Oxepin-Valenztautomerie In: Angewandte Chemie, Band 79, 1967, S. 429–446. doi:10.1002/ange.19670791002.
- Struktur-Wirkungs-Denken in der Chemie – eine Chance für mehr Nachhaltigkeit, Kapitel 5, Industriechemikalien, S. 317 (PDF; 78 kB) (Memento des Originals vom 19. Dezember 2015 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis., abgerufen am 26. März 2013.