3,5-Dibromsalicylsäure
3,5-Dibromsalicylsäure ist eine organische chemische Verbindung, die sowohl zur Stoffgruppe der Phenole als auch zur Stoffgruppe der aromatischen Carbonsäuren gehört. Sie ist damit eine Phenolsäure.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
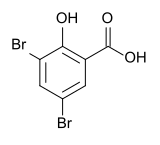 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 3,5-Dibromsalicylsäure | ||||||||||||||||||
| Andere Namen |
3,5-Dibrom-2-hydroxybenzoesäure | ||||||||||||||||||
| Summenformel | C7H4Br2O3 | ||||||||||||||||||
| Kurzbeschreibung |
lange farblose Nadeln[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 295,91 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
löslich in Wasser[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
3,5-Dibromsalicylsäure kann aus Salicylsäure durch Bromierung mit elementarem Brom in Eisessig hergestellt werden.[4]
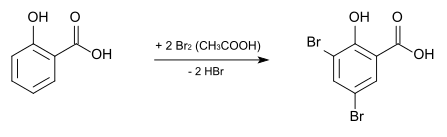
Verwendung
Das Kupfersalz der 3,5-Dibromsalicylsäure wird als Fungizid und als Bakterizid eingesetzt.[5] Ferner ist die 3,5-Dibromsalicylsäure Ausgangsstoff bei der Synthese von Antibiotika.[4]
Reaktionen
Weiteres Bromieren der 3,5-Dibromsalicylsäure führt nach Decarboxylierung zum 2,4,6-Tribromphenol, das seinerseits mit Brom zum 2,4,4,6-Tetrabrom-2,5-cyclohexadienon weiterreagiert.[6] Diese Reaktion kann durch Iodwasserstoff umgekehrt werden.[7]
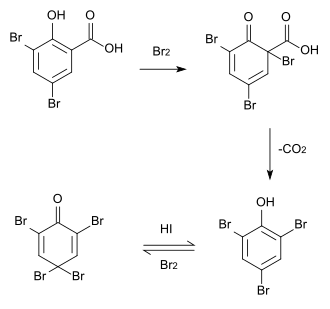
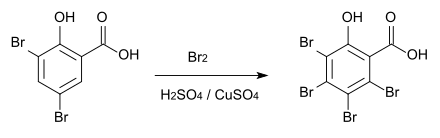
Wird die Reaktion jedoch in Schwefelsäure mit Kupfersulfat als Katalysator durchgeführt, erhält man die 3,4,5,6-Tetrabromsalicylsäure, die sich ab 230 °C zersetzt.[4]
Verbindungen
Das Bariumsalz der 3,5-Dibromsalicylsäure bildet Kristalle der Zusammensetzung (C7H3Br2O3)2Ba · 4 H2O, das Bleisalz ist wasserunlöslich.[1]
Einzelnachweise
- E. Lellmann, R. Grothmann: Ueber einige Derivate der Salicylsäure, in: Chem. Ber., 1884, 17, S. 2724–2731; doi:10.1002/cber.188401702221.
- Eintrag zu 3,5-Dibromsalicylsäure bei ChemBlink, abgerufen am 25. Februar 2011.
- Datenblatt 3,5-Dibromosalicylic acid bei Sigma-Aldrich, abgerufen am 9. Mai 2017 (PDF).
- B. Renneberg, M. Kellner, H. Laatsch: Synthese halogenierter Benzyl- und Benzoylpyrrole, in: Liebigs Ann. Chem., 1993, S. 847–852. doi:10.1002/jlac.1993199301134.
- Patent US3995034A: Biocidal 3,5-dibromosalicylic acid salts. Angemeldet am 3. Oktober 1975, veröffentlicht am 30. November 1976, Anmelder: GAF Corp, Erfinder: Albert F. Strobel.
- John A. Price: The Structure of Tribromophenol bromide, in: J. Am. Chem. Soc., 1955, 77 (20), S. 5436–5437; doi:10.1021/ja01625a081.
- Hans P. Latscha, Helmut A. Klein, Gerald W. Linti: Analytische Chemie: Chemie-Basiswissen III, S. 287 (eingeschränkte Vorschau in der Google-Buchsuche).