2,5-Undecandion
2,5-Undecandion ist eine chemische Verbindung aus der Stoffgruppe der Diketone, bei der die beiden Carbonylgruppen durch zwei Methylengruppen getrennt sind (γ-Diketon).
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
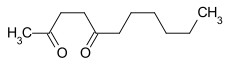 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2,5-Undecandion | ||||||||||||||||||
| Andere Namen |
Undecan-2,5-dion | ||||||||||||||||||
| Summenformel | C11H20O2 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 184,27 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt |
33 °C[1] | ||||||||||||||||||
| Siedepunkt |
141 °C (19 hPa)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
Nach einem von Heinz Hunsdiecker 1942 beschriebenen Syntheseweg lässt sich 2,5-Undecandion ausgehend von 5-Methylfurfurol erhalten. Zunächst wird 5-Methylfurfurol 1 mit Methylpropylketon 2 in einer Aldolkondensation zu der α,β-ungesättigten Carbonylverbindung 3 umgesetzt. Mt Natriumamalgam wird spezifisch nur die Doppelbindung der Seitenkette des Kondensationsprodukts reduziert. Die Zwischenstufe 4 wird anschließen in einer Wolff-Kishner-Reduktion mit Hydrazin in das 2-Methyl-5-hexylfuran 5 überführt. Durch säurekatalysierte Umsetzung bei 120 °C wird der Furanring gespalten und zu 2,5-Undecandion 6 umgesetzt.[3]
.svg.png.webp)
Eine alternative Syntheseroute geht von Heptanal 1 aus. Zunächst wird die Carbonylgruppe mit 1,3-Propandithiol 2 als Dithian 3 geschützt. Das Dithian wird in THF mit n-Butyllithium deprotoniert und mit 1,3-Dichlor-2-buten 4 zur Zwischenstufe 5 alkyliert. Durch Hydrolyse der Dithioacetal-Schutzgruppe mit konzentrierter Schwefelsäure erhält man das 2,5-Undecandion 6. Das Rohprodukt kann durch Derivatisierung mit Girard Reagenz T[4] in Methanol aufgearbeitet und gereinigt werden.[5]
.svg.png.webp)
Verwendung
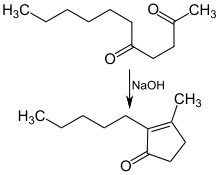
2,5-Undecandion kann in einer Hunsdiecker-Kondensation mit Natronlauge in siedendem Ethanol zu dem Duftstoff Dihydrojasmon cyclisiert werden:[3]
Einzelnachweise
- Eintrag zu Undecane-2,5-dione bei ChemicalBook, abgerufen am 17. März 2020.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Heinz Hunsdiecker: Über das Verhalten der γ-Diketone, I. Mitteilung. In: Berichte der deutschen chemischen Gesellschaft. Band 75, Nr. 5, 6. Mai 1942, S. 447–454, doi:10.1002/cber.19420750502.
- Externe Identifikatoren von bzw. Datenbank-Links zu Girard Reagenz T: CAS-Nummer: 123-46-6, EG-Nummer: 204-629-3, ECHA-InfoCard: 100.004.210, PubChem: 67156, ChemSpider: 60501, Wikidata: Q27285753.
- Tse-Lok Ho, Honor C. Ho, C. M. Wong: A Synthetic Route to Dihydrojasmone; Sulfuric Acid as Dethioacetalization Agent. In: Canadian Journal of Chemistry. 51 (2), 1973, S. 153–155, doi:10.1139/v73-023.