Überspannung (Elektrochemie)
Eine Überspannung ist in der Elektrochemie eine Potentialdifferenz zwischen dem thermodynamischen Redoxpotential einer Halbreaktion und demjenigen Potential, bei der die Redox-Reaktion tatsächlich stattfindet.[1]
| Elektrodenmaterial | Wasserstoff | Sauerstoff | Chlor |
|---|---|---|---|
| Platin (platiniert) | −0,07 V | +0,77 V | +0,08 V |
| Palladium | −0,07 V | +0,93 V | |
| Gold | −0,09 V | +1,02 V | |
| Eisen | −0,15 V | +0,75 V | |
| Platin (glatt) | −0,16 V | +0,95 V | +0,10 V |
| Silber | −0,22 V | +0,91 V | |
| Nickel | −0,28 V | +0,56 V | |
| Graphit | −0,62 V | +0,95 V | +0,12 V |
| Blei | −0,71 V | +0,81 V | |
| Zink | −0,77 V | ||
| Quecksilber | −0,85 V |
Die Überspannung ist daher ein kinetisches Phänomen in der Elektrochemie. Es tritt bei metastabilen Redox-Systemen auf. Dabei laufen Prozesse, die allein aus thermodynamischen Betrachtungen geschehen sollten, aufgrund von kinetischer Hemmung nicht ab.
Ein bekanntes Beispiel ist die Überspannung von Wasserstoff: Nach thermodynamischen Berechnungen müsste sich Eisen in neutralem Wasser auflösen, was aber nicht geschieht. Erst im sauren Milieu, wo die Konzentration der Oxonium-Ionen um mehrere Größenordnungen höher ist, löst sich das Metall auf.
Überspannung bei Elektrolysen
Allgemeines
Das Auftreten von Metastabilität ist bei Redoxprozessen sehr häufig: Nahezu jede organische Substanz ist metastabil und kann nach einer ausreichenden Anregung, z. B. dem Anzünden mit einem Streichholz, in einen stabileren Zustand übergehen. Bei der vollständigen Verbrennung entstehen dabei Wasser, Kohlenstoffdioxid und andere Gase. Entsprechend kann Überspannung als eine Form der Metastabilität auch bei Elektrolysen, also durch einen elektrischen Strom erzwungenen Redoxreaktionen auftreten. Besonders häufig kommt Überspannung bei Reaktionen, die zu einer Entstehung von Gasen wie Wasserstoff führen, vor.
Die Anregung, die dennoch zum Ablauf der Reaktion führt, kann durch eine erhöhte Spannung, die zusätzlich zur Zersetzungsspannung aufgebracht wird, erfolgen. Die Höhe der nötigen Anregung hängt von verschiedenen Aspekten, wie beispielsweise der Art eines entstehenden Gases oder dem Material der Elektroden, ab.
Mikroskopische Gründe für Überspannung
Überspannungen treten auf, wenn mindestens ein Einzelschritt der Elektrolysereaktion kinetisch gehemmt ist, also gebremst wird. Dafür kommen alle Teilschritte des Gesamtprozesses in Frage:
- Die Diffusion der Reaktanten zur Elektrode
- Eine eventuelle Reaktion des Reaktanten vor Erreichen der Elektrode
- Zumindest teilweises Abstreifen der Solvathülle des Reaktanten
- Adsorption des Reaktanten
- Elektronenübergang vom Reaktanten zur Elektrode (Oxidation des Reaktanten) oder andersherum (Reduktion des Reaktanten)
- Desorption des Produkts oder Suchen einer energiearmen Position auf der Oberfläche (bei Abscheidung von Metallen auf demselben Metall) oder Keimbildung (falls sich eine Schicht auf der Elektrode abscheidet)
- Falls das Produkt desorbiert: Bildung und/oder Umstrukturierung der Solvathülle,
- Eventuelle Reaktion des Produkts vor der Elektrode
- Diffusion des Produkts in die Lösung
Weitere Gründe für Überspannung
- Ohm‘sche Überspannung
- Transportüberspannung (Diffusions-, Migrations- und Konvektionsüberspannung)
- Kristallisationsüberspannung
Beispiel
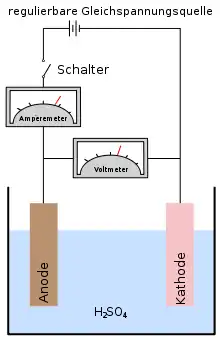
Beispiel an der Elektrolyse einer wässrigen Salzsäure-Lösung mit Graphit-Elektroden. Dabei können sowohl an der Anode als auch an der Kathode jeweils zwei Reaktionen stattfinden:
| Reaktionsort | Gleichung | Potential | Potential + Überspannung |
|---|---|---|---|
| Anode (Oxidation / Elektronenabgabe) | |||
| Kathode (Reduktion / Elektronenaufnahme) | |||
Wenn die Überspannung nicht berücksichtigt wird, müsste folgende Redoxreaktion ablaufen (Elektrolyse des Wassers):
| Gleichung | Potential | |
|---|---|---|
| Gesamtreaktion Redoxreaktion |
||
In der Versuchsdurchführung entsteht jedoch Chlor und Wasserstoff, da bei Berücksichtigung der Überspannung diese Elektrolyse von HCl eine niedrigere Gesamtspannung als die Elektrolyse des Wassers aufweist (siehe Tabellen). Das gleiche Ergebnis erhält man auch mit einer Natriumchlorid-Lösung. Die Natriumionen werden dabei wegen des stark negativen Potentials des Natriums (−2,71 V) nicht zu metallischem Natrium reduziert. Die Wassermoleküle werden wegen der Überspannung nicht zu Sauerstoff oxidiert.
| Gleichung | Potential + Überspannung | |
|---|---|---|
| Gesamtreaktion Redoxreaktion |
||
| Gleichung | Potential + Überspannung | |
|---|---|---|
| Gesamtreaktion Redoxreaktion |
||
Siehe auch
Weblinks
- Elektrolyse – Beispiel zur Überspannung
Einzelnachweise
- Faulkner, Larry R., 1944-: Electrochemical methods : fundamentals and applications. Wiley, 2001, ISBN 978-0-471-04372-0.