Zustandsgröße
Eine Zustandsgröße ist eine makroskopische physikalische Größe, die – ggf. zusammen mit anderen Zustandsgrößen – den Zustand eines physikalischen Systems beschreibt, aber im Rahmen der Betrachtung als Variable angesehen wird. Bleiben alle Zustandsgrößen eines Systems zeitlich konstant, befindet sich das System im thermodynamischen Gleichgewicht oder in einem stationären Fließgleichgewicht. Die Zustandsgrößen beschreiben den aktuellen Zustand eines Systems und sind unabhängig davon, auf welchem Weg es zu diesem Zustand gekommen ist. Ihnen gegenüber stehen Prozessgrößen wie Arbeit und Wärme, die den Verlauf einer Zustandsänderung beschreiben.
In der Thermodynamik betrachtet man
- intensive Zustandsgrößen wie Druck und (absolute) Temperatur
- extensive Zustandsgrößen wie Volumen, Teilchenzahl bzw. Stoffmenge und Entropie
- die thermodynamischen Potentiale: innere Energie, freie Energie, Enthalpie, Gibbs-Energie und das großkanonische Potential, die ebenfalls extensive Zustandsgrößen sind.
Weitere Zustandsgrößen werden daraus abgeleitet.
Einige Zusammenhänge zwischen den Zustandsgrößen werden beschrieben durch die Maxwell-Beziehungen und das Guggenheim-Quadrat.
Klassifizierung
Innerhalb der Zustandsgrößen gibt es zwei grundsätzliche Unterteilungen: zum einen in äußere und innere und zum anderen in intensive und extensive Zustandsgrößen. Unter letzteren zeichnen sich die thermodynamischen Potentiale aus.
Extensive Zustandsgrößen sind Zustandsgrößen, deren Maß mit der Größe des Systems skaliert. Intensive Zustandsgrößen sind Zustandsvariablen, deren Maß nicht von der Größe des Systems abhängt. Teilt man bspw. ein System in zwei in jeder Hinsicht gleiche Teile auf, nimmt jede extensive Zustandsgröße den halben Wert an, wenn man zwei in Bezug auf die Zustandsgröße gleichartige Systeme miteinander vereinigt, nimmt sie den doppelten Wert an. Intensive Zustandsgrößen ändern dadurch ihren Wert nicht.
Beispiel: Die Menge Flüssigkeit in einem Glas ist eine extensive Größe, da zwei Gläser die doppelte Menge Flüssigkeit enthalten. Die Temperatur der Flüssigkeit hingegen ist eine intensive Größe, da zwei Gläser davon nicht doppelt so warm sind wie ein einzelnes.
Zustandsfunktionen oder Thermodynamische Potentiale
Die Thermodynamischen Potentiale innere Energie, freie Energie, Enthalpie und Gibbs-Energie sowie das Großkanonische Potential sind extensive Zustandsgrößen. Sie beschreiben von ihrem Informationsgehalt das thermodynamische System vollständig.
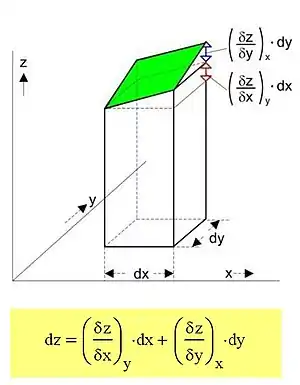
Die thermodynamischen Potentiale misst man gegenüber einem willkürlich festgesetzten Nullpunkt – wie z. B. dem Anfangszustand. Dann entspricht die Änderung der inneren Energie mit den natürlichen Variablen Entropie und Volumen der zugeführten Wärme und Arbeit :
bzw. als vollständiges Differential ausgedrückt:
- .
Sie unterscheiden sich in ihren natürlichen Variablen, die ihrerseits Zustandsgrößen sind und lassen sich mit Hilfe der Legendre-Transformation ineinander überführen. Daraus ergibt sich z. B. die Enthalpie mit deren natürlichen Variablen Entropie und Druck als:
und ihr vollständiges Differential lautet:
- .
Extensive Zustandsvariablen
Bei der Betrachtung der thermodynamischen Potentiale fließen folgende extensive Zustandsgrößen als natürliche Variablen ein: Volumen, Entropie und Teilchenzahl bzw. Stoffmenge. In dynamischen oder von energiespeichernden Feldern beeinflussten Systemen sind auch die …ströme oder …flüsse extensive Zustandsgrößen.
Intensive Zustandsgrößen
Bei der Betrachtung der thermodynamischen Potentiale fließen folgende intensive Zustandsvariablen als natürliche Variablen ein: Druck, (absolute) Temperatur und chemisches Potential. Die Änderung einer intensiven Größe hat immer die Änderung des thermodynamischen Gleichgewichts zur Folge. In dynamischen oder von energiespeichernden Feldern beeinflussten Systemen sind auch die Geschwindigkeiten und Feldstärken intensive Zustandsgrößen.
Kombinationen
Kombinationen aus intensiven Zustandsgrößen desselben Zustands sind wiederum intensive Zustandsgrößen. Solche aus einer extensiven und einer intensiven Größe sind extensiv. Solche Kombinationen treten als Differenz der thermodynamischen Potentiale auf. In diesem Zusammenhang wird immer eine Größe mit ihrer jeweils konjugierten Größe multipliziert. Ein Beispiel hierfür ist die Verschiebearbeit . Sie stellt die Differenz zwischen der Enthalpie und der inneren Energie dar. Sie trägt zwar den Namen einer …arbeit ist aber im Gegensatz zu anderen …arbeiten keine Prozessgröße.
Zusammenhänge
Zustandsgleichungen
Experimentelle Befunde zeigen, dass die genannten Größen nicht unabhängig voneinander geändert werden können, was auch in der Gibbssche Phasenregel bzw. in der Festlegung des Zustands eines Systems auf eine bestimmte Anzahl Freiheitsgrade zum Ausdruck kommt. Die entsprechenden Zusammenhänge zwischen den Zustandsgrößen eines Systems beschreiben Zustandsgleichungen.
Gase unter normalen Bedingungen lassen sich durch Ideales Gas annähernd beschreiben. Es gilt die Allgemeine Gasgleichung
mit der allgemeinen Gaskonstante .
Eine bessere Näherung für reale Gase bringt die Van-der-Waals-Gleichung:
- .
Maxwell-Beziehungen
Die Maxwell-Beziehungen oder Maxwell-Relationen der Thermodynamik (nach dem Physiker James Clerk Maxwell) beschreiben die Zusammenhänge zwischen Änderungen der verschiedenen Zustandsgrößen, so lässt sich z. B. die Änderung der Temperatur oder Entropie mit Hilfe der Änderungen anderer Zustandsgrößen, z. B. Druck oder Volumen , ausdrücken:
Guggenheim-Quadrat
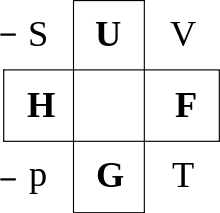
Das Guggenheim-Quadrat oder Guggenheim-Schema ist ein Hilfsmittel, um einige einfache, aber grundlegende Beziehungen der Thermodynamik aus dem Gedächtnis heraus aufzustellen. Sie lassen sich sowohl auf die Maxwell-Beziehungen als auch auf die charakteristischen Funktionen anwenden. Verknüpft werden die Entropie S, die innere Energie U, das Volumen V, die freie Energie F (auch Helmholtz-Energie A), die Temperatur T, die Gibbs-Energie G, der Druck p, und die Enthalpie H.
Es ist nach Edward Guggenheim benannt.
Merkhilfen für drei Freiheitsgrade
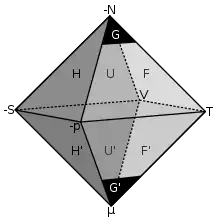
Das Guggenheim-Quadrat beschreibt Systeme mit zwei Freiheitsgraden. Für drei Freiheitsgrade wurden Merkhilfen in Form der geometrischen Figuren Oktaeder[1][2] und Kuboktaeder[3] beschrieben. Bei diesen sind, im Gegensatz zum Quadrat, die thermodynamischen Potentiale (G, U, H, A etc.) keine Kanten, sondern Flächen.
Literatur
- Literatur zur Technischen Thermodynamik
- Jibamitra Ganguly: Thermodynamics in earth and planetary sciences. 2008, Thermodynamic Square: A Mnemonic Tool, S. 59–60 (Google Books [abgerufen am 15. September 2011]).
- Wedler, Gerd: Lehrbuch der Physikalischen Chemie. 2. Auflage. VCH, 1985, ISBN 978-3-527-29481-7, 2.3.2 – Charakteristische thermodynamische Funktionen, S. 252–256.
Weblinks
- The Guggenheim scheme. Archiviert vom Original am 24. Juli 2007; abgerufen am 15. September 2011 (englisch).
Einzelnachweise
- L. T. Klauder. In: American Journal of Physics, 1968, 36(6), S. 556–557, doi:10.1119/1.1974977
- James M. Phillips. In: J. Chem. Educ., 1987, 64(8), S. 674–675, doi:10.1021/ed064p674
- Ronald. F. Fox. In: J. Chem. Educ., 1976, 53(7), S. 441–442, doi:10.1021/ed053p441