Thermodynamisches Potential
Thermodynamische Potentiale sind in der Thermodynamik Größen, die von ihrem Informationsgehalt her das Verhalten eines thermodynamischen Systems im Gleichgewicht vollständig beschreiben.[1] Die unabhängigen Zustandsvariablen eines thermodynamischen Potentials bezeichnet man dann als dessen natürliche Variablen, wenn deren Ableitung des Potentials gleich einer der abhängigen Zustandsvariablen ist (beispielsweise: ).[2] Ein thermodynamisches Potential entspricht vom Informationsgehalt der inneren Energie ,[1] deren natürliche Variablen alle extensiv sind (Fundamentalgleichung).
Thermodynamische Potentiale, die Energien sind, lassen sich durch Legendre-Transformation aus der inneren Energie herleiten, haben jedoch anders als diese eine oder mehrere intensive Größen als natürliche Variablen . Die intensiven Größen entstehen bei der Koordinatentransformation als Ableitungen der inneren Energie nach ihren extensiven Variablen.
Daneben gibt es weitere thermodynamische Potentiale, die keine Energien sind, beispielsweise die Entropie .[1]
Der Begriff des thermodynamischen Potentials wurde von Gottfried Falk zum Begriff der Massieu-Gibbs-Funktionen (nach Josiah Willard Gibbs) verallgemeinert, bei denen es sich um entsprechende Zustandsfunktionen in nicht notwendigerweise thermodynamischen Systemen handelt.[3][4]
Physikalische Bedeutung
Ein Extremwert (nicht immer ein Minimum) eines thermodynamischen Potentials zeigt das thermodynamische Gleichgewicht an.
So hat sich nach dem Anschluss eines abgeschlossenen Systems an ein anderes ein thermodynamisches Gleichgewicht eingestellt, sobald die Entropie des Gesamtsystems maximal ist. In diesem Fall sind auch alle intensiven Parameter der beiden Systeme jeweils gleich:
Außerdem fassen thermodynamische Potentiale die Zustandsgleichungen des Systems zusammen, da diese durch Differenzieren eines thermodynamischen Potentiales nach seinen abhängigen Variablen zugänglich sind.[5]
Beschreibung
Die innere Energie und die aus ihr mittels Legendre-Transformation hervorgehenden Funktionen sind thermodynamische Potentiale (bis auf die Ausnahme , s. u.). Die Legendre-Transformation transformiert die Potentiale
- von Entropie nach Temperatur , da
- von Volumen nach Druck , da
- von Teilchenzahl nach chemisches Potential , da
Aufgrund dieser 3 Variablenpaare gibt es mögliche thermodynamische Potentiale:
| Name (Alternativname) | Formelzeichen | natürliche Variablen (intensive fett) |
Charakteristische Funktion f | Zusammenhänge |
|---|---|---|---|---|
| Innere Energie | (Eulergleichung für die innere Energie) | |||
| Freie Energie (Helmholtz-Potential) |
||||
| Enthalpie | ||||
| Gibbs-Energie (Freie Enthalpie) |
||||
| - | ||||
| Großkanonisches Potential | ||||
| - | ||||
| - | Nicht sinnvoll, da die Gibbs-Duhem-Relation die unabhängige Vorgabe der Variablen verbietet.[6] |
Alle sinnvollen thermodynamischen Potentiale, die aus U(S,V,N) durch Legendre-Transformation hervorgehen, liefern die gleiche, vollständige Information über ein System. Die einfachste Beschreibung des Systems liefert jedoch je nach Ensemble nur eines der Potentiale; dies ist im Gleichgewicht extremal.
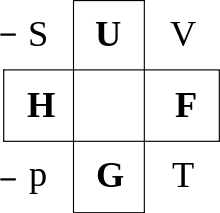
Eine Möglichkeit, sich die thermodynamischen Potentiale mit ihren natürlichen Variablen zu merken, ist das Guggenheim-Quadrat.
Beispiel für Transformation
Exemplarisch soll der Wechsel von einem Potential zum anderen mittels charakteristischer Funktionen (totaler Differentiale) durchgeführt werden.
Ziel ist, von der inneren Energie U mit den natürlichen Variablen auf ein neues Potential mit den natürlichen Variablen zu transformieren. Wir beginnen bei der inneren Energie:
Mit
folgt
Nun bringe auf die linke Seite:
Das neue Potential hängt nun von den natürlichen Variablen ab und wird „freie Energie “ genannt. Es ist die Legendretransformierte von U(S,V,N) bezüglich der Variablen S.
Zustandsgleichungen
Sei ein beliebiges thermodynamisches Potential, dann kann sein totales Differential geschrieben werden als
wobei
- die natürlichen Variablen von sind und
- die jeweils dazu konjugierten Variablen.
Aus der Kettenregel folgt:
Hier ist die Menge aller natürlichen Variablen von ohne . Die sind Ausdrücke thermodynamischer Parameter in Abhängigkeit von Ableitungen des thermodynamischen Potentials, das von seinen natürlichen Variablen abhängt. Die sind also gerade die Zustandsfunktionen des Systems.[7]
Einzelnachweise
- Wolfgang Nolting: Grundkurs Theoretische Physik. Band 6: Statistische Physik. 6. Auflage. Springer, Berlin u. a. 2007, ISBN 978-3-540-68870-9, S. 373 ff., (Google Books).
- Wolfgang Nolting: Grundkurs Theoretische Physik. Band 4: Spezielle Relativitätstheorie, Thermodynamik. 6., aktualisierte Auflage. Springer, Berlin u. a. 2005, ISBN 3-540-24119-1, S. 206.
- Gottfried Falk: Theoretische Physik. Auf der Grundlage einer allgemeinen Dynamik (= Heidelberger Taschenbücher. ). 2 Bände (Bd. 1: Elementare Punktmechanik. Bd. 2: Allgemeine Dynamik, Thermodynamik. 7 und 27, ISSN 0073-1684). Springer, Berlin u. a. 1966–1968.
- Gottfried Falk, Wolfgang Ruppel: Energie und Entropie. Eine Einführung in die Thermodynamik. Springer, Berlin u. a. 1976, ISBN 3-540-07814-2.
- Christoph Strunk: Moderne Thermodynamik. 2015, S. 144 ff., (Google Books).
- Walter Greiner, Ludwig Neise, Horst Stöcker: Thermodynamik und statistische Mechanik (= Theoretische Physik. Bd. 9). 2., völlig überarbeitete und erweiterte Auflage. Deutsch, Thun u. a. 1993, ISBN 3-8171-1262-9, S. 150.
- Callen: Thermodynamics and an Introduction to Thermostatistics. 2nd edition. 1985, S. 37.
Literatur
- Herbert B. Callen: Thermodynamics and an Introduction to Thermostatistics. 2nd edition. Wiley & Sons, New York NY u. a. 1985, ISBN 0-471-86256-8.
- Ulrich Nickel: Lehrbuch der Thermodynamik. Eine anschauliche Einführung. 3., überarbeitete Auflage. PhysChem, Erlangen 2019, ISBN 978-3-937744-07-0.
- Christoph Strunk: Moderne Thermodynamik. Von einfachen Systemen zu Nanostrukturen. de Gruyter, Berlin u. a. 2015, ISBN 978-3-11-037105-5, (Google Books).