Xylenole
Die Xylenole oder Dimethylphenole bilden in der Chemie eine Gruppe aromatischer Verbindungen mit zwei Methylgruppen und einer Hydroxygruppe. Man kann sie als Hydroxyderivate der Xylole oder Dimethylderivate des Phenols auffassen. Es existieren somit sechs Isomere. Der Name Xylenol leitet sich aus der Kombination der Namen der Aromaten Xylen und Phenol ab.
Vorkommen
Alle Xylenole finden sich im Steinkohlenteer und Buchenholzteer und sind ein Bestandteil des Stoffgemisches Kreosot.[1] 3,5-Xylenol kommt natürlich im Tamarindenbaum (Tamarindus indica) vor.[2]
Struktur und Eigenschaften
Die physikalischen Eigenschaften der sechs Xylenol-Isomere ähneln einander. Die Xylenole sind in Wasser zumeist nur sehr wenig löslich. Sie bilden farblose bis gelbliche Nadeln oder Platten mit stechendem Geruch.[3] Chemisch verhalten sie sich wie typische Phenole, so bilden sie zum Beispiel in alkalischer Lösung Phenolate, die eine bedeutend höhere Wasserlöslichkeit besitzen.
Die Methylgruppen üben einen (schwachen) +I-Effekt auf den Aromaten aus, wodurch die Elektronendichte im Ring erhöht wird. Dadurch wird u. a. die Acidität des phenolischen OH abgeschwächt. Die pKs-Werte sind daher etwas höher als die des Phenols (9,99[4]) und auch der Kresole.
| Xylenole | |||||||||||
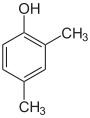
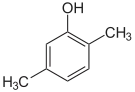
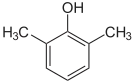
| Name | 2,3-Xylenol | 2,4-Xylenol | 2,5-Xylenol | 2,6-Xylenol | 3,4-Xylenol | 3,5-Xylenol | |||||
| Andere Namen | 2,3-Dimethyl- phenol, vic.-o-Xylenol 2,3-XYLENOL (INCI)[5] |
2,4-Dimethyl- phenol, asym.-m-Xylenol |
2,5-Dimethyl- phenol, p-Xylenol 2,5-XYLENOL (INCI)[6] |
2,6-Dimethyl- phenol, vic.-m-Xylenol 2,6-XYLENOL (INCI)[7] |
3,4-Dimethyl- phenol, asym.-o-Xylenol |
3,5-Dimethyl- phenol, sym.-m-Xylenol | |||||
| Strukturformel | 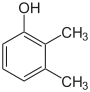 |
 |
 |
 |
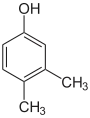 |
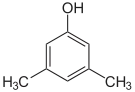 | |||||
| CAS-Nummer | 526-75-0 | 105-67-9 | 95-87-4 | 576-26-1 | 95-65-8 | 108-68-9 | |||||
| 1300-71-6 (Isomerengemisch)[3] | |||||||||||
| PubChem | 10687 | 7771 | 7267 | 11335 | 7249 | 7948 | |||||
| FL-Nummer | 04.065 | 04.066 | 04.019 | 04.042 | 04.048 | 04.020 | |||||
| Summenformel | C8H10O | ||||||||||
| Molare Masse | 122,17 g·mol−1 | ||||||||||
| Aggregatzustand | fest, Isomerengemisch meist flüssig | ||||||||||
| Kurzbeschreibung | farblose bis gelbliche Nadeln oder Platten mit stechendem Geruch[3] | ||||||||||
| Schmelzpunkt | 73–75,5 °C[8] | 24 °C[9] | 75–77 °C[10] | 46–48 °C[11] | 65–68 °C[12] | 61 °C[13] | |||||
| Siedepunkt | 216 °C[8] | 210 °C[9] | 212 °C[10] | 203 °C[11] | 226 °C[12] | 219 °C[13] | |||||
| pKs-Wert[4] | 10,50 | 10,45 | 10,22 | 10,59 | 10,32 | 10,15 | |||||
| Löslichkeit | wenig löslich in Wasser (2,6-Xylenol: gut bis sehr gut wasserlöslich[11], 3,4-Xylenol: mischbar[12]), gut löslich in Ethanol und Ether | ||||||||||
| GHS- Kennzeichnung |
|
| |||||||||
| H- und P-Sätze | 301‐311‐314‐411 | 301‐311‐314 | |||||||||
| keine EUH-Sätze | keine EUH-Sätze | ||||||||||
| 273‐280 305+351+338‐310[8] |
280‐273 302+352‐301+330+331 305+351+338‐309+310[9] |
273‐280 309+310‐302+352 305+351+338[10] |
280‐273 302+352‐301+330+331 305+351+338‐309+310[11] |
273‐280 301+330+331‐302+352 305+351+338‐309+310[12] |
280 305+351+338‐310[13] | ||||||
Darstellung
Xylenole können in der Regel aus den Xylidinen durch Diazotierung und anschließende Verkochung des Diazoniumsalzes dargestellt werden.
Verwendung
Zusammen mit den Kresolen und Kresolsäuren sind Xylenole eine wichtige Klasse von Phenolen mit großer industrieller Bedeutung. Xylenole werden als Ausgangsstoffe zur Synthese von Pestiziden, Antioxidantien und Pharmazeutika (z. B. Mexiletin) verwendet. 2,5-Xylenol (p-Xylenol) dient als Grundlage zur Darstellung der pH-Indikatoren Xylenolphthalein, Xylenolblau und Bromxylenolblau. Vom 2,6-Xylenol leiten sich Metallphthalein und Xylenolorange ab, sie werden als Indikatoren in der Komplexometrie eingesetzt. 2,6-Xylenol dient als Ausgangsstoff für die Synthese von Polyphenylenether. Durch Chlorierung von 3,5-Xylenol ist das Desinfektionsmittel Chlorxylenol zugänglich.[14]
Weblinks
Einzelnachweise
- H. P. T. Ammon, C. Hunnius: Hunnius pharmazeutisches Wörterbuch, Verlag Walter de Gruyter 2004, ISBN 3-11-017475-8, S. 867.
- 3,5-DIMETHYLPHENOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 6. Januar 2022.
- Eintrag zu CAS-Nr. 1300-71-6 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 15. Dezember 2013. (JavaScript erforderlich)
- CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- Eintrag zu 2,3-XYLENOL in der CosIng-Datenbank der EU-Kommission, abgerufen am 1. Oktober 2021
- Eintrag zu 2,5-XYLENOL in der CosIng-Datenbank der EU-Kommission, abgerufen am 18. January 2022.
- Eintrag zu 2,6-XYLENOL in der CosIng-Datenbank der EU-Kommission, abgerufen am 17. September 2021.
- Eintrag zu CAS-Nr. 526-75-0 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 15. Dezember 2013. (JavaScript erforderlich)
- Eintrag zu CAS-Nr. 105-67-9 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 15. Dezember 2013. (JavaScript erforderlich)
- Eintrag zu CAS-Nr. 95-87-4 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 15. Dezember 2013. (JavaScript erforderlich)
- Eintrag zu CAS-Nr. 576-26-1 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 15. Dezember 2013. (JavaScript erforderlich)
- Eintrag zu CAS-Nr. 95-65-8 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 15. Dezember 2013. (JavaScript erforderlich)
- Eintrag zu CAS-Nr. 108-68-9 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 15. Dezember 2013. (JavaScript erforderlich)
- Hagers Handbuch der pharmazeutischen Praxis, S. 921 (eingeschränkte Vorschau in der Google-Buchsuche).


