Tubocurarin
Tubocurarin ist ein Nervengift. Als Hauptbestandteil von Tubocurare zählt es zu den Pfeilgiften, die zusammenfassend als Curare bezeichnet werden. Diese gehören zu der Stoffklasse der Alkaloide. Der Name leitet sich vom spanischen "Tubo" (dt. Rohr) ab, da es früher in Bambusrohren gelagert wurde.[4]
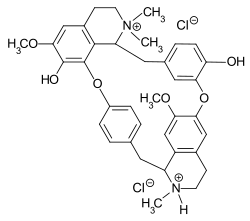
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Tubocurarin | |||||||||||||||
| Summenformel | C37H41N2O6 | |||||||||||||||
| Kurzbeschreibung |
gelblicher Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code |
M03AA02 | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 609,73 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
löslich in Wasser[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Vorkommen
Tubocurarin kommt unter anderem in Chondrodendron tomentosum und anderen Pflanzen der Gattung vor.[5]
Wirkungsweise
Tubocurarin besetzt kompetitiv die nicotinischen Acetylcholinrezeptoren der postsynaptischen Membran. Es erfolgt eine Blockierung der ligandengesteuerten Natrium-Ionenkanäle, wobei keine Depolarisation ausgelöst wird. Tubocurarin lähmt die quergestreifte Muskulatur des Bewegungsapparates und wird als nicht-depolarisierendes Muskelrelaxans bezeichnet.
Pharmazie
Als pharmazeutischer Wirkstoff wird Tubocurarin als Chlorid-Hydrochlorid-Pentahydrat[6] eingesetzt.[7] Im Präparat Intocostrin fand es 1942 Anwendung zur Muskelrelaxierung bei der Narkose.[8] Eine vergleichbare Wirkung wird mit Suxamethonium (etwa im Präparat Lysthenon) erzielt.
Toxikologie
Zur Behandlung von Tubocurarinvergiftungen werden häufig Acetylcholinesterase-Hemmer eingesetzt. Diese verhindern, dass Acetylcholin im Synaptischen Spalt von der Acetylcholinesterase hydrolytisch in Essigsäure und Cholin gespalten wird. Dadurch wird die Konzentration an Acetylcholin im synaptischen Spalt erhöht. Das Verhältnis des Agonisten Acetylcholin und seinem Antagonisten Tubocurarin wird also in Richtung des Acetylcholins verschoben, wodurch die Wirkung des Tubocurarins abgeschwächt wird, da Acetylcholin somit verhältnismäßig öfter an die nicotinischen Acetylcholinrezeptoren bindet und diese aktiviert.[9]
Einzelnachweise
- Eintrag zu Tubocurarindichlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 6. Februar 2017. (JavaScript erforderlich)
- Datenblatt (+)-Tubocurarine chloride pentahydrate bei Sigma-Aldrich, abgerufen am 25. April 2011 (PDF).
- Datenblatt Tubocurarin bei Acros, abgerufen am 26. Februar 2010.
- Norman G. Bisset: War and hunting poisons of the New World. Part 1. Notes on the early history of curare. In: Journal of Ethnopharmacology. Band 36, Nr. 1, Februar 1992, S. 1–26, doi:10.1016/0378-8741(92)90056-W (elsevier.com [abgerufen am 4. Juli 2021]).
- Wink, Michael; Ben-Erik van Wyk; Coralie Wink, Handbuch der giftigen und psychoaktiven Pflanzen. Wissenschaftliche Verlagsgesellschaft, Stuttgart, 2008.
- Externe Identifikatoren von bzw. Datenbank-Links zu Tubocurarin Chlorid Hydrochlorid Pentahydrat: CAS-Nummer: 6989-98-6, EG-Nummer: 615-023-7, ECHA-InfoCard: 100.108.489, GESTIS-Stoffdatenbank: 531432, PubChem: 23422, ChemSpider: 21902, Wikidata: Q27271261.
- Eintrag zu Tubocurarine in der DrugBank der University of Alberta, abgerufen am 9. Dezember 2018.
- Erich Kirchner: Vorbemerkung. In: Erich Kirchner, Wolfgang Seitz (Hrsg.): Klinik der Muskelrelaxation. 50 Jahre nach Griffith und Johnson. Steinkopff, Darmstadt 1994; Neudruck ebenda 2012, ISBN 978-3-642-95978-3, S. 1.
- W C Bowman: Neuromuscular block: Neuromuscular block. In: British Journal of Pharmacology. Band 147, S1, Januar 2006, S. S277–S286, doi:10.1038/sj.bjp.0706404, PMID 16402115 (wiley.com [abgerufen am 4. Juli 2021]).