Thulium(II)-iodid
Thulium(II)-iodid ist eine anorganische chemische Verbindung des Thuliums aus der Gruppe der Iodide.
| Kristallstruktur | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
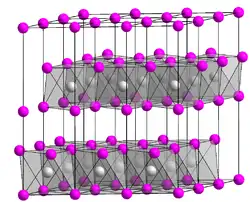 | |||||||||||||
| _ Tm2+ _ I− | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Thulium(II)-iodid | ||||||||||||
| Andere Namen |
Thuliumdiiodid | ||||||||||||
| Verhältnisformel | TmI2 | ||||||||||||
| Kurzbeschreibung | |||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 422,74 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Löslichkeit |
löslich in Tetrahydrofuran[3] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Gewinnung und Darstellung
Thulium(II)-iodid kann durch Reduktion von Thulium(III)-iodid mit Thulium im Vakuum bei 800 bis 900 °C gewonnen werden.[2]
Auch die Darstellung durch Reaktion von Thulium mit Quecksilber(II)-iodid ist möglich.[2]
Ebenfalls möglich ist die direkte Darstellung aus Iod und Thulium.[4]
Eigenschaften
Thulium(II)-iodid ist ein schwarzer Feststoff. Die Verbindung ist äußerst hygroskopisch und kann nur unter sorgfältig getrocknetem Schutzgas oder im Hochvakuum aufbewahrt und gehandhabt werden. An Luft geht Thulium(II)-iodid unter Feuchtigkeitsaufnahme in Hydrate über, die aber instabil sind und sich mehr oder weniger rasch unter Wasserstoff-Entwicklung in Oxidiodide verwandeln. Mit Wasser spielen sich diese Vorgänge noch sehr viel schneller ab. Die Verbindung besitzt eine Kristallstruktur vom Cadmium(II)-iodid-Typ.[2]
Verwendung
Thulium(II)-iodid wird zur Förderung der Kreuzkupplung von 2-Acetylthiophen oder Ethyl-2-thiophencarboxylat mit Aldehyden und Ketonen in Tetrahydrofuran bei Raumtemperatur verwendet. Es wird auch als Reduktionsmittel ähnlich wie Samarium(II)-iodid benutzt.[1]
Einzelnachweise
- Datenblatt Thulium(II) iodide, anhydrous, powder, ≥99.9% bei Sigma-Aldrich, abgerufen am 2. Mai 2014 (PDF).
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 1081.
- Karl A. Jr. Gschneidner, Jean-Claude Bunzli, Vitalij K. Pecharsky: Handbook on the Physics and Chemistry of Rare Earths. Elsevier, 2009, ISBN 0-08-093257-6, S. 258 (eingeschränkte Vorschau in der Google-Buchsuche).
- Karl A. Jr. Gschneidner, Jean-Claude Bunzli, Vitalij K. Pecharsky: Handbook on the Physics and Chemistry of Rare Earths. Elsevier, 2009, ISBN 0-08-093257-6, S. 247 (eingeschränkte Vorschau in der Google-Buchsuche).
