Tetraethylammoniumion
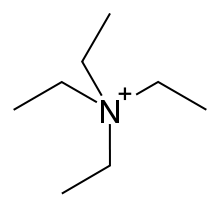
Das Tetraethylammoniumion ist ein einwertiges Kation mit der Summenformel C8H20N+ (Halbstrukturformel (C2H5)4N+). Es besteht aus einem Stickstoffatom welches tetraedrisch von vier Ethylresten umgeben ist und gehört somit zur Gruppe der quartären Ammoniumverbindungen. Formal leitet es sich vom Ammoniumion durch Substitution der Wasserstoffatome durch Ethylreste ab. Das Tetraethylammoniumion gehört zu den schwach-koordinierenden Kationen.[1] Es existieren eine große Anzahl von Tetraethylammoniumsalzen, der allgemeinen Formel C8H20NX, wobei X ein einwertiges Anion darstellt.
Darstellung
Tetraethylammoniumsalze können durch Umsetzung von Triethylamin mit substituierten Ethylverbindungen dargestellt werden, wobei der Substituent eine Abgangsgruppe ist, welches dann meist als Gegenion des Salzes fungiert.
- Reaktion von Triethylamin mit Ethyliodid zu Tetraethylammoniumiodid.[2]
Das Gegenion kann jedoch auch anschließend ausgetauscht werden:
- Reaktion von Tetraethylammoniumbromid mit Silbertetrafluoroborat zu Tetraethylammoniumtetrafluoroborat unter Ausfällung von Silberbromid.[3]
Verwendung
Es ist ein Nervengift, das u. a. in der Neurophysiologie benutzt wird, um in Experimenten an Neuronen die Kaliumkanäle zu blockieren.[4] TEA blockiert die spannungsaktivierten Kaliumkanäle, die für Repolarisation des Membranpotentials nach einem Aktionspotential benötigt werden.
Salze
Tetraethylammonium bildet mit Anionen Salze. Wichtige sind unter anderem:
- Tetraethylammoniumbromid
- Tetraethylammoniumchlorid
- Tetraethylammoniumcyanid[5]
- Tetraethylammoniumhydroxid[6]
- Tetraethylammoniumiodid
- Tetraethylammoniumnitrat[7]
- Tetraethylammoniumperfluoroctansulfonat[8]
Literatur
- Peter Deetjen: Physiologie. 4. Auflage. Urban & Fischer, 2007, ISBN 978-3-437-44440-1, S. 15. (eingeschränkte Vorschau in der Google-Buchsuche)
Einzelnachweise
- K. O. Christe, W. W. Wilson: Reaction of the fluoride anion with acetonitrile. Chloroform and methylene chloride. In: J. Fluorine Chem. 47, 1990, S. 117–120
- F. M. Menger, U. V. Venkataram: Proximity as a component of organic reactivity. In: J. Am. Chem. Soc. 107, 1985, S. 4706–4709.
- K. Fukui, K. Ohkubo, T. Yamabe: The Catalytic Activity of Onium Compounds in the Homogeneous Liquid Phase Oxidation of Cumene and α-Pinene. In: Bull. Chem. Soc. Jpn. 42, 1969, S. 312–318.
- B. Roux: Extracellular blockade of potassium channels by TEA+: the tip of the iceberg? In: J Gen Physiol. 128(6), Dec 2006, S. 649–657. PMID 17130517
- Externe Identifikatoren von bzw. Datenbank-Links zu Tetraethylammoniumcyanid: CAS-Nummer: 13435-20-6, EG-Nummer: 236-566-2, ECHA-InfoCard: 100.033.228, PubChem: 3014735, Wikidata: Q83026984.
- Externe Identifikatoren von bzw. Datenbank-Links zu Tetraethylammoniumhydroxid: CAS-Nummer: 77-98-5, EG-Nummer: 201-073-3, ECHA-InfoCard: 100.000.977, GESTIS-Stoffdatenbank: 492413, PubChem: 6509, ChemSpider: 6263, Wikidata: Q27288030.
- Externe Identifikatoren von bzw. Datenbank-Links zu Tetraethylammoniumnitrat: CAS-Nummer: 1941-26-0, EG-Nummer: 217-725-5, ECHA-InfoCard: 100.016.114, PubChem: 74744, Wikidata: Q72504985.
- Externe Identifikatoren von bzw. Datenbank-Links zu Tetraethylammoniumperfluoroctansulfonat: CAS-Nummer: 56773-42-3, EG-Nummer: 260-375-3, ECHA-InfoCard: 100.054.869, GESTIS-Stoffdatenbank: 146734, PubChem: 92531, ChemSpider: 83538, Wikidata: Q72481197.