Syntin
Syntin ist ein Raketentreibstoff auf der Basis eines Kohlenwasserstoffs mit der Summenformel C10H16, der drei hochgespannte Cyclopropanringe enthält.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
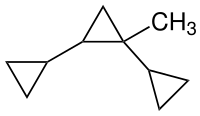 | |||||||||||||
| Stereoisomerengemisch ohne Angabe der Stereochemie | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Syntin | ||||||||||||
| Andere Namen |
1′-Methyl-1,1′:2′,1′′-tercyclopropan | ||||||||||||
| Summenformel | C10H16 | ||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 136,23 g·mol−1 | ||||||||||||
| Dichte |
0,8504 g·cm−3[1] | ||||||||||||
| Siedepunkt | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Darstellung und Gewinnung
Die Synthese von Syntin erfolgt in einer mehrstufigen Synthesesequenz, in der die einzelnen Cyclopropyleinheiten gebildet und verknüpft werden.[1] Als Ausgangsverbindung kann das Hydroxypropylmethylketon verwendet werden, aus dem nach Umwandlung zum Chlorid durch nucleophile Substitution und anschließender Zyklisierung unter schwach basischen Bedingungen mit dem Cyclopropylmethylketon die erste Cyclopropyleinheit gebildet wird. Eine anschließende Dimerisierung in Gegenwart von Aluminiumtri-tert.-butylat führt zum 1,3-Dicyclopropyl-2-buten-1-on.[3] Durch eine Umsetzung mit Hydrazinhydrat erhält man das 3,5-Dicyclopropyl-5-methyl-4,5-dihydro-1H-pyrazol. Aus diesem wird durch eine Destillation über Kaliumhydroxid bei 190 °C unter Stickstoffabspaltung der zentrale Cyclopropylring und somit die Zielverbindung gebildet. Aus der Synthese resultiert ein Isomerengemisch.
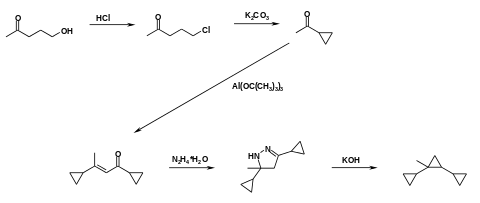
Eine Trennung der Isomere kann mittels präparativer Chromatographie erfolgen.[4]
Eigenschaften
Syntin ist eine farblose Flüssigkeit, die als Isomerengemisch unter Normaldruck bei 158 °C siedet.[1] Unter reduziertem Druck von 6,5 kPa wird ein Siedepunkt von 80 °C beobachtet.[1] Wegen der drei hochgespannten Cyclopropanringe hat das Molekül eine hohe Bildungsenthalpie von ΔfH°(l)= 131,6 kJ·mol−1 bzw. 966 kJ·kg−1 für das trans-Isomer sowie ΔfH°(l)= 134,1 kJ·mol−1 bzw. 984 kJ·kg−1 für das cis-Isomer.[4] Es handelt sich somit um eine endotherme Verbindung mit einer hohen Verbrennungsenthalpie von −6353,7 kJ·mol−1 für das trans-Isomer bzw. −6355,9 kJ·mol−1 für das cis-Isomer.[4] Die Vorteile gegenüber herkömmlichen Kohlenwasserstoffen wie RP-1 bestehen in der größeren Dichte, geringeren Viskosität und der größeren Verbrennungswärme.[5]
Stereochemie
Syntin enthält zwei Stereozentren an einem Cyclopropanring, so dass zwei trans- und zwei cis-Isomere existieren. In der Praxis ist nur das Gemisch der vier Stereoisomere relevant:
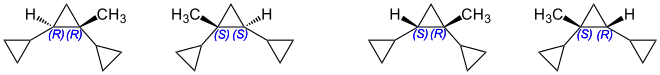
Verwendung
Syntin wurde in der Sowjetunion und in Russland in den 1980er und 1990er Jahren als Treibstoff für die Sojus-Rakete und den Buran eingesetzt. Zuerst wurde es in der UdSSR 1960 synthetisiert, und in den 1970er Jahren begann die Massenproduktion. Es wurde in einem mehrstufigen synthetischen Prozess aus gewöhnlichen Kohlenwasserstoffen hergestellt. Nach dem Zerfall der Sowjetunion wurde die Produktion dieser Substanz zu teuer und daher eingestellt.
Einzelnachweise
- A. P. Mesheheryakov, V. G. Glukhovtsev, A. D. Petrov: „Synthesis of 1-methyl-1,2-dicyclopropylcyclopropane“ in Doklady Akademii Nauk SSSR 130 (1960) 779–781.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- L.I. Smith, J.S. Showell: Cyclopropanes. XIV. Incidental Experiments and an Attemt to Synthesize Dicyclopropyl in J. Org. Chem. 17 (1952) 839–844, doi:10.1021/jo01140a009.
- S.M. Pimenova, M.P. Kozina, V.P. Kolesov: The enthalpies of combustion and formation of cis- and trans-1-methyl-1,2-dicyclopropylcyclopropane in Thermochim. Acta 221 (1993) 139-141, doi:10.1016/0040-6031(93)80531-E.
- В. Азов, Д. Воронцов: Последний бой углеводородов? (Memento vom 4. Mai 2014 im Internet Archive) in Новостей космонавтики 18 (2008) 44–46.
Literatur
- A. P. Mesheheryakov, V. G. Glukhovtsev, A. D. Petrov: „Synthesis of 1-methyl-1,2-dicyclopropylcyclopropane“, Doklady Akademii Nauk SSSR, 1960, 130, S. 779–781.
- Yu. P. Semenov, B. A. Sokolov, S. P. Chernykh, A. A. Grigor'ev, O. M. Nefedov, N. N. Istomin, G. M. Shirshov: „Multiple strained-ring alkane as high-performance liquid rocket fuel“, RU 2233385, C2 20040727.
- T. Edwards: „Liquid Fuels and Propellants for Aerospace Propulsion: 1903-2003“, Journal of Propulsion and Power, 2003, 19(6), S. 1089–1107.
- V. Azov, D. Vorontsov: „The last battle of hydrocarbons?“, Novosti Kosmonavtiki, 2008, 18, No. 2 (301), S. 44–46.