Propanidid
Propanidid ist ein Derivat des im Gewürznelkenöl enthaltenen Eugenols.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
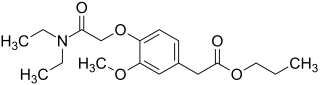 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Propanidid | |||||||||||||||||||||
| Andere Namen |
Propyl {4-((diethylcarbamoyl)methoxy)-3-methoxyphenyl}acetat | |||||||||||||||||||||
| Summenformel | C18H27NO5 | |||||||||||||||||||||
| Kurzbeschreibung |
blassgelbes Öl[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
N01AX04 | |||||||||||||||||||||
| Wirkstoffklasse |
Benzolderivat | |||||||||||||||||||||
| Wirkmechanismus |
Kurznarkotikum | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 337,40 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||||||||
| Siedepunkt | ||||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Eigenschaften
Propanidid wurde mit Cremophor-EL als Lösungsvermittler für intravenöse Kurznarkosen unter dem Markennamen Epontol angewandt. 1962 wurde es von Bayer patentiert[1] und 1965 zur klinischen Anwendung zugelassen. Es verteilte sich im Körper schnell und bewirkte ein angenehmes Einschlafen und rasches Erwachen nach drei bis vier Minuten.[3] Es war daher für chirurgische Kurzeingriffe (etwa Einrenkungen) gut geeignet.
Synthese
Eugenol wird zunächst acetyliert; anschließend wird das Acetat oxidiert, wobei die Doppelbindung des Eugenols gespalten wird und 4-Acetoxy-3-Methoxyphenylessigsäure entsteht. Die Acetylgruppe wird wieder abgespalten; anschließend wird die freie Säure mit Propanol verestert. Zuletzt wird die phenolische Hydroxygruppe mit Chloressigsäurediethylamid im Sinne einer Williamson-Ethersynthese umgesetzt.[4]
Literatur
- Michael Fresenius; Michael Heck: Repetitorium Anästhesiologie: Für die Facharztprüfung und das Europäische Diplom (German Edition), 5., vollst. aktualisierte Aufl.. Auflage, Springer-Verlag, Berlin 2007, ISBN 978-3-540-46575-1, S. 642 (Abgerufen am 2. Dezember 2009).
Weblinks
- Eintrag zu Propanidid bei Vetpharm
- Eintrag zu Propanidid in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
Anmerkungen
- Eintrag zu Propanidid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Dezember 2014.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Vgl. Wolfgang Wirth, F. Hoffmeister: Pharmakologische Untersuchungen mit Propanidid. In: Die intravenöse Kurznarkose mit dem neuen Phenoxyessigsäure-Derivat Propanidid. Springer, 1965.
- Eberhard Schröder, Clemens Rufer, Ralph Schmiechen: Arzneimittelchemie I. Georg Thieme Verlag, 1976, ISBN 3-13-520601-7.