Pivalinsäure
Pivalinsäure ist eine verzweigte, kurzkettige Carbonsäure aus der Gruppe der vier isomeren Pentansäuren, sowie die einfachste Koch-Säure (tertiäre gesättigte Monocarbonsäuren).
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
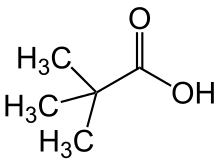 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Pivalinsäure | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C5H10O2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Kristalle mit unangenehmem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 102,13 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
0,91 g·cm−3 (20 °C)[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
163–164 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| pKS-Wert |
5,03 (20 °C)[4] | ||||||||||||||||||
| Löslichkeit |
wenig in Wasser (25 g·l−1 bei 20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
Synthetisch kann Pivalinsäure durch Oxidation von Pinacolon, durch Grignard-Reaktion aus tert-Butylchlorid (untere Darstellung) oder durch die Koch-Reaktion aus 2-Methylpropen (Isobuten), Kohlenstoffmonoxid und Wasser erhalten werden:
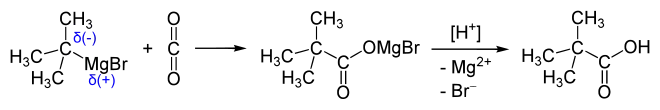
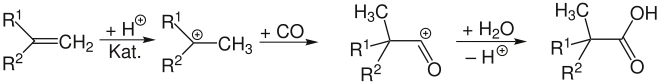
Eigenschaften
Die Pivalinsäure bildet farblose, nadelförmige Kristalle von stechendem Geruch, die sich wenig in Wasser, aber gut in Ethanol und Diethylether lösen. Durch sterische Effekte auf das Molekül weist Pivalinsäure im Vergleich zu anderen Valeriansäuren einige besondere Eigenschaften auf, z. B. ist die Esterbildung bzw. die Hydrolyse der Pivalinsäureester erheblich erschwert.
Verwendung
Pivalinsäure wird zur Herstellung von Polyvinylestern (Vinylpivalat) und pharmazeutischen Präparaten verwendet. Dabei nutzt man den Effekt der sterischen Hemmung durch Einsatz von Estern medizinisch wirksamer Substanzen aus, die dann im Organismus nur langsam gespalten und resorbiert werden, wie z. B. Testosteronpivalat.[2] Weiterhin wird Pivalinsäure as Co-Katalysator in Palladium-katalysierten Reaktionen (zumeist C-H Aktivierungsreaktionen) verwendet.[5][6]
Sicherheitshinweise
Pivalinsäure ist brennbar, die Zündtemperatur liegt bei ca. 500 °C, der Flammpunkt im geschlossenen Tiegel bei 64 °C. Die Säure reizt Augen, Atemwege, Schleimhäute und Haut und kann auch über die Haut resorbiert werden.[2]
Einzelnachweise
- Jürgen Falbe, Manfred Regitz: RÖMPP Lexikon Chemie. Band 2: Cm–G, 10. Auflage, Thieme, 1997, ISBN 3-13-734710-6, S. 991.
- Eintrag zu 2,2-Dimethylpropionsäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 22. Februar 2017. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-220.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Dissociation Constants of Organic Acids and Bases, S. 8-44.
- Marc Lafrance, Keith Fagnou: Palladium-catalyzed benzene arylation: incorporation of catalytic pivalic acid as a proton shuttle and a key element in catalyst design. In: Journal of the American Chemical Society. 128, Nr. 51, 27. Dezember 2006, ISSN 0002-7863, S. 16496–16497. doi:10.1021/ja067144j. PMID 17177387.
- Dongbing Zhao, Weida Wang, Shuang Lian, Fei Yang, Jingbo Lan, Jingsong You: Phosphine-Free, Palladium-Catalyzed Arylation of Heterocycles through CH Bond Activation with Pivalic Acid as a Cocatalyst. In: Chemistry – A European Journal. 15, Nr. 6, 26. Januar 2009, ISSN 0947-6539, S. 1337–1340. doi:10.1002/chem.200802001.
Weblinks
- Eintrag zu Pivalinsäure. In: P. J. Linstrom, W. G. Mallard (Hrsg.): NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD.
- International Chemical Safety Card (ICSC) für Pivalic Acid beim National Institute for Occupational Safety and Health (NIOSH)

