Perrheniumsäure
Perrheniumsäure ist eine anorganische chemische Verbindung aus der Gruppe der Säuren. Sie liegt nur in wässriger Lösung vor. Als feste Perrheniumsäure wird Dirheniumdihydratoheptoxid Re2O7(OH2)2 bezeichnet.[5]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
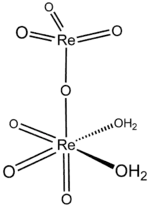 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Perrheniumsäure | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | HReO4 | ||||||||||||||||||
| Kurzbeschreibung |
farblose bis schwach gelbliche Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 251,21 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig (Lösung in Wasser)[2] | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| pKS-Wert |
−1,25[4] | ||||||||||||||||||
| Löslichkeit |
mischbar mit Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Eine wässrige Perrheniumsäure-Lösung kann durch Reaktion von Rhenium mit Wasserstoffperoxid gewonnen werden.[3]
Ebenfalls möglich ist die Darstellung durch Auflösung von Rhenium(VII)-oxid in Wasser.[3]
Die Lösungen können nur bis zu einer Konzentration von max. 70 Gewichtsprozent HReO4 eingedampft werden, darüber verflüchtigt sich HReO4.[3]
Feste Perrheniumsäure kann aus einer wässrigen möglichst konzentrierten Perrheniumsäure-Lösung gewonnen werden, indem im Exsikkator mittels Phosphorpentoxid oder Magnesiumperchlorat diese vom Wasserüberschuss befreit wird.[3]
Eigenschaften
Perrheniumsäure ist als Reinstoff nicht darstellbar und nur als farblose bis schwach gelbliche Lösung existent.[1] Dirheniumdihydratoheptoxid ist ein schwach gelblicher, äußerst hygroskopischer Feststoff. Er ist löslich in Nitromethan und zersetzt sich bei 65 °C unter Verflüchtigung von HReO4. Er besitzt eine monokline Kristallstruktur mit der Raumgruppe P21/m (Raumgruppen-Nr. 11) und den Gitterparametern a = 882 pm, b = 889 pm, c = 503 pm und β = 112,0°, mit O3Re-O-ReO3(OH2)2-Molekülen.[3]
Verwendung
Perrheniumsäure dient zur Darstellung gut leitender und supraleitender synthetischer Metalle.[2]
Einzelnachweise
- Datenblatt Perrhenic acid, 75-80% aq. soln. bei AlfaAesar, abgerufen am 2. August 2013 (PDF) (JavaScript erforderlich).
- Datenblatt Perrhenic acid solution, 75-80 wt. % in H bei Sigma-Aldrich, abgerufen am 2. August 2013 (PDF).
- Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1632.
- Eintrag zu Perrhenate. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. September 2018.
- H. Beyer, O. Glemser, B. Krebs, G. Wagner: Die Struktur von Dirheniumdihydratoheptoxid Re2O7(OH2)2. - Ein neuer Typ von Wasserbindung in einem Aquoxid -. In: Zeitschrift für anorganische und allgemeine Chemie. 376, 1970, S. 87, doi:10.1002/zaac.19703760111.
