Natriumtetraborat
Natriumtetraborat ist eine chemische Verbindung des Natriums aus der Gruppe der Borate.
| Kristallstruktur | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
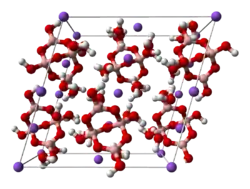 | |||||||||||||
| _ Na+ _ B3+ _ O2− _ H+ | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Natriumtetraborat | ||||||||||||
| Andere Namen | |||||||||||||
| Verhältnisformel | Na2B4O7 | ||||||||||||
| Kurzbeschreibung |
farbloser geruchloser Feststoff[3] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 201,22 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[3] | ||||||||||||
| Dichte | |||||||||||||
| Schmelzpunkt | |||||||||||||
| Siedepunkt |
1575 °C (Zersetzung)[6] | ||||||||||||
| Dampfdruck | |||||||||||||
| Löslichkeit | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: fortpflanzungsgefährdend (CMR)[8] | ||||||||||||
| MAK |
Schweiz: 0,8 mg·m−3 (gemessen als einatembarer Staub)[9] | ||||||||||||
| Toxikologische Daten | |||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||
| ΔHf0 |
−3291,1 kJ/mol[10] | ||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Vorkommen
Natriumtetraborat kommt natürlich in Form der Minerale Borax (Decahydrat), Tincalconit (Pentahydrat) und Kernit (Tetrahydrat) vor.[11] Es kommt auch als Bestandteil von Salzsolen (z. B. im Searles-See in Kalifornien) vor.[2]
Gewinnung und Darstellung
Natriumtetraborat-Anhydrat kann durch Entwässerung der Hydrate in zwei Schritten (Calcinieren und anschließendes Schmelzen) gewonnen werden. Schnelles Abkühlen ergibt ein amorphes Produkt, beim langsamen Abkühlen entsteht die α-Form (rhombische Kristalle).[2]
Eigenschaften
Natriumtetraborat ist ein farbloser geruchloser Feststoff, der wenig löslich in Wasser ist. Er zersetzt sich bei Erhitzung über 1575 °C, wobei sich Boroxid und Natriumoxid bilden.[3] Das Decahydrat gibt bei 75 °C Kristallwasser ab[5] und löst sich bei raschem Erhitzen im eigenen Kristallwasser auf. Bei langsamem Erhitzen verliert es einen Teil seines Kristallwassers und bildet ein Pentahydrat. Bei etwa 400 °C spaltet diese weiteres Kristallwasser ab und man erhält wasserfreies Natriumtetraborat.[12] Bei der Entwässerung können insgesamt zehn mol Wasser abgespalten werden. Acht stammen aus dem Kristallwasser, zwei aus dem [B4O5(OH)4]2−-Anion. Dieses Anion kennt man erst seit Aufklärung der Kristallstruktur Mitte des 20. Jahrhunderts.[13] Erhitzt man dieses wiederum weiter, schmilzt es ab 742 °C zu einer glasartigen Schmelze.
In dieser Schmelze lösen sich zahlreiche Metalloxide unter der Bildung charakteristischer Färbungen und bilden nach dem Abkühlen eine glasige Perle (Boraxperle). Mineralsäuren setzen Borsäure aus Natriumtetraborat frei.[12] Das Tetrahydrat kann durch Erwärmen eines Gemisches aus gleichen Teilen von Natriumtetraborat-Pentahydrats und Natriumtetraborat-Decahydrat auf 120 °C gewonnen werden.[14] Das Anhydrat hat eine trikline Kristallstruktur mit der Raumgruppe P1 (Raumgruppen-Nr. 2), das Pentahydrat eine trigonale Kristallstruktur mit der Raumgruppe R3 (Raumgruppen-Nr. 146) und das Decahydrat eine monokline Kristallstruktur mit der Raumgruppe C2/c (Raumgruppen-Nr. 15).[4]
Beim Lösen in Wasser bildet sich jeweils Borsäure.[15]
Verwendung
Natriumtetraborat wird als Flussmittel beim Hartlöten und als Holzschutzmittel gegen Pilz- und Insektenbefall eingesetzt. Es ist in Seifen und Pudern gegen fettige Haut, Bleichcremes und verschiedenen Hautpflegemitteln enthalten. Es wird zur Herstellung von Gläsern, Glasfaserisolierungen, Glasfasermatten, Emaille, Borsäure und Natriumperborat verwendet. Ferner für Glasuren, zum Steifen von Geweben und als Flammschutzausrüstung von Holz und Textilien eingesetzt.[3]
Toxikologie
Natriumtetraborat wird aufgrund seiner Reproduktionstoxizität seit Juni 2010 als Substance of Very High Concern eingestuft.[8]
Einzelnachweise
- Eintrag zu E 285: Sodium tetraborate (borax) in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 27. Juni 2020.
- Franz v Bruchhausen, Siegfried Ebel, Eberhard Hackenthal, Ulrike Holzgrabe: Hagers Handbuch der Pharmazeutischen Praxis: Folgeband 5: Stoffe L-Z. Springer-Verlag, 2013, ISBN 978-3-642-58388-9, S. 299 (eingeschränkte Vorschau in der Google-Buchsuche).
- Eintrag zu Natriumtetraborat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2018. (JavaScript erforderlich)
- Jean de Ans, Ellen Lax: Taschenbuch für Chemiker Und Physiker: Band 3: Elemente, Anorganische … Springer DE, 1998, ISBN 3-540-60035-3, S. 602 (eingeschränkte Vorschau in der Google-Buchsuche).
- Datenblatt di-Natriumtetraborat-Decahydrat (PDF) bei Merck, abgerufen am 27. November 2012.
- Datenblatt di-Natriumtetraborat (PDF) bei Merck, abgerufen am 27. November 2012.
- Eintrag zu Disodium tetraborate, anhydrous im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 18. Oktober 2015.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 7440-42-8), abgerufen am 21. Dezember 2019.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-6.
- mindat.org: Search Minerals By Chemistry
- Seilnacht: Borax
- N. Morimoto, Mineral J. (Sapporo) 2 (1956) 1. Chem. Abstr. 52 (1958) 12687
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 809.
- europa.eu: Annex XV Dossier von Dinatriumtetraborat, wasserfrei (PDF; 363 kB)

