NO-Synthasen
Das Enzym Stickstoffmonoxid-Synthase, kurz NO-Synthase (NOS), katalysiert die Bildung von Stickstoffmonoxid (NO) aus der Aminosäure L-Arginin. Es kommt in den meisten Eukaryoten, aber auch in manchen Bakterien vor. NO hat im Organismus in Abhängigkeit von Zielstruktur und Konzentration eine Vielzahl von physiologischen Aufgaben, aber nur eine Halbwertszeit von fünf Sekunden, weswegen es ständig neu hergestellt werden muss. Beim Menschen sind drei Isoformen der NO-Synthase bekannt, die von unterschiedlichen Genen codiert werden. Mutationen in einem dieser Gene (NOS1) können Pylorusstenose Typ 1 (IHPS1) zur Folge haben.[1]
| Stickstoffmonoxid-Synthase | ||
|---|---|---|
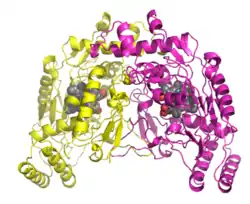
| ||
| Kristallstruktur der menschlichen Stickstoffmonoxid-Synthase nach PDB 1nsi | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 1200–1400 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homodimer | |
| Kofaktor | Häm, FAD, FMN, Tetrahydrobiopterin | |
| Isoformen | NOS1, NOS2, NOS3 | |
| Bezeichner | ||
| Gen-Namen | 1nsi , NOS1, NOS2, NOS3 | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 1.14.13.39, Monooxygenase | |
| Reaktionsart | Dihydroxylierung | |
| Substrat | L-Arginin + n NADPH + m O2 | |
| Produkte | L-Citrullin + NO + n NADP+ + m H2O | |
| Vorkommen | ||
| Homologie-Familie | NO-Synthase | |
| Übergeordnetes Taxon | Lebewesen | |
| Ausnahmen | Archaeen | |
Isoformen
Man unterscheidet -je nach Einteilung- drei oder vier Isoformen der NOS:
1. eNOS in den Zellen an der Innenseite von Blutgefäßen (Endothelzellen): NO bewirkt indirekt, durch Erhöhung des cGMP (Cyclisches Guanosinmonophosphat)-Spiegels, die Relaxation der glatten Gefäßmuskulatur, was zu einer Vasodilatation und damit zu einer Absenkung der Nachlast des Herzens und des Blutdrucks führt. Durch diese Reaktion wurde die Wirkungsweise einer ganzen Gruppe von Medikamenten verständlich, darunter Amylnitrit, Nitroprussid und Nitroglycerin. Diese Medikamente setzen NO im Körper frei. Der gleiche Mechanismus liegt bei der diätetischen Behandlung von Arteriosklerose-Patienten mit Arginin selbst zugrunde. Das gasförmige NO wird im Rahmen spezieller Herzkatheteruntersuchungen verabreicht, um die Reaktion der Lungengefäße darauf zu testen.
2. iNOS in Makrophagen/Mikrogliazellen: Eine weitere Wirkung von NO ist der Schutz des Körpers vor Eindringlingen. So produzieren Makrophagen große Mengen von NO, das Bakterien und Zellen abtötet. Eine übermäßige Produktion von NO durch die Makrophagen kann auch Nebenwirkungen haben. So ist die gefährliche Absenkung des Blutdrucks bei einem septischen Schock zu erklären.
3. nNOS in Neuronen: NO ist auch im Gehirn (Kopfteil des Zentralnervensystems, kurz ZNS) nachweisbar. Dort übernimmt es die Funktion eines Neurotransmitters, wobei es unter anderem die Synthese von cGMP erhöht. Das kleine Molekül kann leicht in Zellen hinein- und hinausdiffundieren, da es membrangängig ist. Man vermutet auch, dass NO, bedingt durch seine schnelle Diffusion, relativ große Areale des ZNS modulieren kann.
4. mtNOS in Mitochondrien: mtNOS ist ein Stoffwechselmodulator für Synthese, Proliferation, Apoptose und Regulation des Sauerstoffverbrauchs. Die Einordnung als eigene Isoform ist fraglich, da die mtNOS eher als eine Splicing-Variante der nNOS angesehen wird.
Expression
eNOS und nNOS sind im menschlichen Körper konstitutiv exprimiert (ständig vorhanden), weshalb sie manchmal (veraltet) auch gemeinsam als cNOS (constitutive NOS) bezeichnet werden – im Gegensatz nur iNOS, die zwar auch konstitutiv, insbesondere jedoch nach Aktivierung durch Transkriptionsfaktoren vermehrt exprimiert wird.
Durch Bakteriengifte (Endotoxine) oder proinflammatorische Cytokine wird die iNOS induziert. Die bekanntesten Induktoren der iNOS in Makrophagen sind IFN-γ, Tumornekrosefaktor-α, Interleukin-1β sowie bakterielle Lipopolysaccharide.
Katalysierte Reaktion
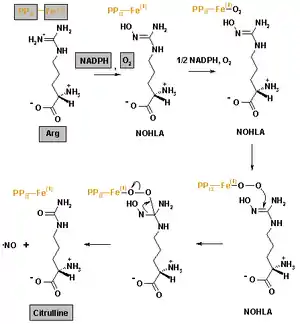
Es handelt sich um die Fünf-Elektronen-Oxidation (siehe Reaktionsschema) eines der Guanidino-Stickstoffatome von L-Arginin, die in zwei Schritten mit dem Intermediat NOHLA abläuft.[2]
Bei der Reaktion wird L-Citrullin abgespalten, so dass man diese Reaktion auch als Kurzschluss des Harnstoffzyklus – unter Umgehung der Intermediate Ornithin und Argininosuccinat – betrachten kann.
Regulation der Aktivität
eNOS und nNOS
Da beide mischfunktionellen Oxidasen ständig im Organismus vorhanden sind, muss ihre Aktivität einem strengen Regulationsmechanismus unterliegen. Es konnte jedoch beim Corpus pineale der Ratte gezeigt werden, dass die nNOS durchaus auch induzierbar ist. Bei Ratten, deren zirkadiane Rhythmik durch Dauerlicht gestört wurde, war ein fast vollständiges Verschwinden der nNOS in den Zellen des Corpus pineale zu beobachten. Hier bleibt zu vermuten, dass der Organismus der Ratte die Produktion eines für die Regulation nicht mehr nötigen Moleküls abschaltet, anstatt dessen Aktivität herabzusetzen.
eNOS
Die Aktivität der eNOS im Gefäßendothel ist zwar auch von mechanischen Kräften (Schubspannung) abhängig, überragende Bedeutung hat jedoch die Regulation über die intrazelluläre Calciumkonzentration. Die aktive Form der eNOS besteht aus einem heterogenen Tetramer aus zwei Monomeren eNOS Molekülen und zwei Ca2+/Calmodulin-Komplexen. Bei niedriger intrazellulärer Calciumionen-Konzentration bildet sich diese aktive Form nicht aus, kann aber alternativ durch Phosphorylierung auch bei Ruhe-Calciumionen-konzentrationen aktiviert werden.
iNOS
Im Gegensatz dazu ist die Aktivität der iNOS kaum reguliert, sodass es nach Exprimierung zu einer schnellen, starken und langanhaltenden NO Synthese kommt. Die von der iNOS produzierte Menge an NO kann um das 1000-fache höher sein als durch die konstitutive eNOS. In dieser hohen Konzentration wirkt NO zytotoxisch und dient damit z. B. den Makrophagen zur Immunabwehr. Bei einer Sepsis kann dies jedoch problematische Folgen haben, da NO auch eine Rolle bei der Regulation der Gefäßweite spielt.
Konkurrenz mit Arginase
Eine Hemmung der durch die iNOS vermittelten NO-Synthese kann über die Verfügbarkeit des Substrates L-Arginin erreicht werden, beispielsweise durch Erhöhung der Expression der extrahepatischen Form des kompetitiven Enzyms Arginase, welche L-Arginin zu L-Ornithin und Harnstoff spaltet und durch die Interleukine 4,10 und 13 sowie bakterielle Lipopolysaccharide induziert wird.
Neutrophile Granulozyten modulieren die Immunantwort durch Sekretion von Arginase. In Psoriasisläsionen wird Arginase überexprimiert. Dies führt zu verminderter Verfügbarkeit von Stickstoffoxid im Gewebe, da Arginase mit NO-Synthase um Arginin konkurriert. Dieselbe Konkurrenz innerhalb von Makrophagen wird von intrazellulären Pathogenen wie Mycobacterium tuberculosis, Toxoplasma gondii und anderen ausgenutzt, um der Immunreaktion zu entgehen.[3][4][5]
Einzelnachweise
- UniProt P29475
- PROSITE documentation PDOC60001. Swiss Institute of Bioinformatics (SIB), abgerufen am 20. September 2011 (englisch).
- Jacobsen LC, Theilgaard-Mönch K, Christensen EI, Borregaard N: Arginase 1 is expressed in myelocytes/metamyelocytes and localized in gelatinase granules of human neutrophils. In: Blood. 109, Nr. 7, April 2007, S. 3084–7. doi:10.1182/blood-2006-06-032599. PMID 17119118.
- Bruch-Gerharz D, Schnorr O, Suschek C, et al.: Arginase 1 overexpression in psoriasis: limitation of inducible nitric oxide synthase activity as a molecular mechanism for keratinocyte hyperproliferation. In: Am. J. Pathol. 162, Nr. 1, Januar 2003, S. 203–11. PMID 12507903. PMC 1851107 (freier Volltext).
- El Kasmi KC, Qualls JE, Pesce JT, et al.: Toll-like receptor-induced arginase 1 in macrophages thwarts effective immunity against intracellular pathogens. In: Nat. Immunol.. 9, Nr. 12, Dezember 2008, S. 1399–406. doi:10.1038/ni.1671. PMID 18978793.
Literatur
- Robert F. Schmidt, Florian Lang: Physiologie des Menschen mit Pathophysiologie. 30. Auflage, Springer Medizin Verlag, Heidelberg 2007.
- Werner Müller-Esterl: Biochemie – Eine Einführung für Mediziner und Naturwissenschaftler. Elsevier GmbH, München 2004.