N-Methyltaurin
N-Methyltaurin oder 2-Methylaminoethansulfonsäure ist eine Aminosulfonsäure, die wie eine Aminosäuren in kristallinem Zustand und in polaren Lösungsmitteln als Zwitterion vorliegt.[2] Im Gegensatz zum weit verbreiteten Taurin wurde N-Methyltaurin in der Natur bisher nur in Rotalgen gefunden,[3] wo es durch Methylierung von Taurin gebildet wird. Es eignet sich wegen seiner hohen Polarität und der relativ guten Löslichkeit seiner Erdalkalimetallsalze zur Veresterung (eigentlich Amidbildung) mit langkettigen Carbonsäuren zu Tauriden (Acylaminoethansulfonaten), die als milde anionische Tenside eingesetzt werden.[4]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | N-Methyltaurin | ||||||||||||||||||
| Andere Namen |
2-Methylamino-ethansulfonsäure | ||||||||||||||||||
| Summenformel | C3H9NO3S | ||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 139,17 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
246–249 °C[1] | ||||||||||||||||||
| Löslichkeit |
löslich in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Die Synthese des N-Methyltaurins wurde bereits 1878[5] berichtet, wobei Methylamin mit dem Silbersalz der 2-Chlorethansulfonsäure zur Reaktion gebracht wurde. Eine naheliegende Variante ist die Umsetzung des Natriumsalzes der 2-Chlorethansulfonsäure mit Methylamin.[6] Addition von Methylamin an Natriumvinylsulfonat in wässriger Lösung ergibt nach dem Ansäuern mit Essigsäure N-Methyltaurin in 85%iger Ausbeute.[7] Die Reinigung der Reaktionsmischung und Darstellung des N-Methyltaurins kann auch durch Passage der Natriumsalzlösung über ein Kationenaustauscherharz in seiner H-Form und anschließend über ein Anionenaustauscherharz in seiner OH-Form erfolgen.[8] Die Reaktion von Natriumisethionat mit Methylamin in Wasser bei hoher Temperatur und Druck liefert das Natriumsalz des N-Methyltaurins,[9]
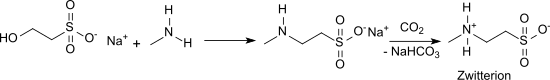
aus dem nach Sättigung mit CO2 und Abtrennung des ausfallenden Natriumhydrogencarbonats reines N-Methyltaurin gewonnen wird.[10]
Eigenschaften
N-Methyltaurin ist ein weißer pulverförmiger Feststoff, der in Wasser leicht löslich ist. Aus chinesischen Quellen kommt auch das Natriumsalz des N-Methyltaurins in Form gelblicher Kristalle und 60–65 Gew.%ige farblose, alkalisch reagierende Lösungen in den Handel.
Verwendung
N-Methyltaurin bzw. sein Natriumsalz findet als polare Kopfgruppe in Tensiden aus der Klasse der Tauride (Acylaminoethansulfonaten), gelegentlich auch Methyltaurate genannt, Verwendung. Die Tauride zeichnen sich durch exzellente Schaumbildung – auch in Gegenwart von Öl und Hautfetten – und Schaumstabilität mit guter Hautverträglichkeit und breiter pH-Stabilität aus.[11] Der Marktdurchbruch für N-Methyltaurin als Haarwuchsmittel steht noch aus.[12]
Einzelnachweise
- Eintrag zu N-Methyltaurin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Januar 2019. (JavaScript erforderlich)
- J.A. Kalaitzis et al., Zwitterionic 2-(methylamino)ethanesulfonic acid, Acta Cryst. (2003). E59, o726-o727, doi:10.1107/S160053680300895X
- B. Lindberg, Methylated Taurines and Choline Sulfate in Red Algae, Acta Chem. Scand., 9, 1955, S. 1323–1326.
- E.W. Flick, Cosmetic Additives: An Industrial Guide, Noyes Publication, Park Ridge, New Jersey, 1991, ISBN 0-8155-1255-4, S. 352.
- Dittrich, E. (1878), Ueber Methyltaurin und die Bildung von Methyltaurocyamin und Taurocyamin, J. Prakt. Chem., 18: 63–78. doi:10.1002/prac.18780180102.
- J.W. Schick, E.F. Degering, Synthesis of Taurine and N-Methyltaurine, Ind. Eng. Chem., 39, 7 (1947), S. 906–909, doi:10.1021/ie50451a024.
- Patent US7049464: Process for producing of an aminoalkylsulfonic acid and a method of salt exchange for a salt thereof. Veröffentlicht am 23. Mai 2006, Anmelder: Wako Pure Chemical Industries, Ltd., Erfinder: T. Kimura et al..
- Patent US2693488: Purification of amino alkane sulfonic acids by ion exchange. Veröffentlicht am 2. November 1954, Anmelder: The Dow Chemical Co., Erfinder: A.R. Sexton.
- Patent US1932907: Veröffentlicht am 31. Oktober 1933, Anmelder: I.G. Farbenindustrie AG, Erfinder: O. Nicodemus, W. Schmidt.
- Deutsches Patentamt, Auslegeschrift 1 122 540; Erfinder: E. Elbel et al.; Anmelder: Farbwerke Hoechst AG, bekanntgemacht am 27. Januar 1962.
- Clariant-Broschüre: Mild Surfactants, (pdf; 801 kB)
- Patent EP1235574: Veröffentlicht am 28. August 2002, Anmelder: Shiseido Co. Ltd., Erfinder: C. Hamada et al..
