Mevalonatweg
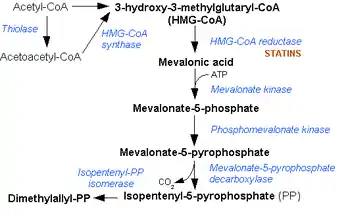
Der Mevalonatweg ist ein Stoffwechselweg in Eukaryoten, über den von Acetyl-CoA ausgehend die Biosynthese von Isoprenoiden erfolgt und damit der Aufbau von Steroiden und Sekundärmetaboliten ermöglicht wird. Endprodukt des Mevalonatwegs ist nach sechs Schritten Isopentenylpyrophosphat (IPP) und Dimethylallylpyrophosphat (DMAPP), die Ausgangsstoffe im Menschen für die Cholesterinbiosynthese und die Steroidbiosynthese. Teile des Mevalonatwegs finden im Zytosol und in den Peroxisomen statt.
| Übergeordnet |
| Phospholipid-Biosynthese |
| Gene Ontology |
|---|
| QuickGO |
Die meisten Bakterien benutzen zur Synthese von Isoprenoiden den Methylerythritolphosphatweg, vielen stehen aber auch die Enzyme des Mevalonatwegs zur Verfügung. Archaeen hingegen nutzen ausschließlich den Mevalonatweg in einer leicht veränderten Reihenfolge, bei der Phosphomevalonat zuerst zu Isopentenylphosphat decarboxyliert und dann weiter zum IPP phosphoryliert wird.[1][2]
Reaktionsschritte
Acetoacetyl-CoA
Der Mevalonatweg beginnt in den Mitochondrien mit der Übertragung eines Acetylrests von Acetyl-CoA auf ein zweites Acetyl-CoA-Molekül. Dieses von dem zytosolischen Enzym Acetyl-CoA-Acetyltransferase (ACAT2) katalysierte Reaktionsgleichgewicht ist außerdem Teil der beta-Oxidation, des Auf- und Abbaus von Ketokörpern und mancher Aminosäuren.
![]() +
+ ![]() CoA-SH +
CoA-SH + ![]()
Zwei Moleküle Acetyl-CoA werden zu Coenzym A und Acetoacetyl-CoA umgesetzt und umgekehrt.
HMG-CoA
Die Verknüpfung eines weiteren Moleküls Acetyl-CoA mit Acetoacetyl-CoA zu 3-Hydroxy-3-methylglutaryl-CoA (HMG-CoA) in den Mitochondrien benötigt die zytosolische Isoform des Enzyms HMG-CoA-Synthase (HMGCS1).
![]() +
+ ![]()
![]() + CoA-SH
+ CoA-SH
Acetoacetyl-CoA wird zu HMG-CoA acetyliert.
R-Mevalonat
Die HMG-CoA-Reduktase ist ein Membranprotein am endoplasmatischen Retikulum, das die Reduktion von HMG-CoA zu Mevalonat katalysiert. Dieser Schritt ist geschwindigkeitsbestimmend für den Mevalonatweg, und damit auch beispielsweise für den Aufbau von Cholesterin.
![]() + 2 NADPH/H+
+ 2 NADPH/H+ ![]() + CoA-SH + 2 NADP+
+ CoA-SH + 2 NADP+
HMG-CoA wird zu Mevalonat reduziert.
5-Phospho-R-mevalonat
Die Phosphorylierung von Mevalonat mithilfe der Mevalonatkinase findet im Zytosol statt.
![]() + ATP
+ ATP ![]() + ADP
+ ADP
R-Mevalonat wird zu 5-Phospho-R-mevalonat umgesetzt. Ein Molekül ATP wird verbraucht.
5-Diphospho-R-mevalonat
Eine weitere Phosphorylierung führt zum 5-Pyrophosphomevalonat. Katalysator ist hier die Phosphomevalonat-Kinase, die bisher nur in den Peroxisomen gefunden wurde.
![]() + ATP
+ ATP ![]() + ADP
+ ADP
5-Phospho-R-mevalonat wird zu 5-Diphospho-R-mevalonat umgesetzt.
Isopentenylpyrophosphat
Der letzte Reaktionsschritt zum IPP stellt die von der Diphosphomevalonat-Decarboxylase katalysierte Decarboxylierung von Diphosphomevalonat dar. Sie findet im Zytosol statt.
![]() + ATP
+ ATP ![]() + ADP + Pi + CO2
+ ADP + Pi + CO2
5-Diphospho-R-mevalonat wird zu Isopentenylpyrophosphat (IPP) umgesetzt.
Dimethylallyldiphosphat
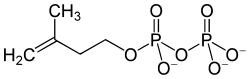
Die wechselseitige Isomerisierung von IPP zu DMAPP und umgekehrt wird von der Isopentenyldiphosphat-Isomerase katalysiert. Beide Isoformen des Enzyms wurden in Peroxisomen lokalisiert.
![]()
Isopentenyldiphosphat (auch -pyrophosphat) (IPP) und Dimethylallyldiphosphat (auch -pyrophosphat) (DMAPP) gehen ineinander über.
Literatur
- N. Qureshi, W. Porter: Conversion of acetyl-coenzyme A to isopentenyl pyrophosphate. In: J. W. Porter, S. L. Spurgeon (Hrsg.): Biosynthesis of Isoprenoid Compounds. Vol 1. John Wiley & Sons, New York 1981, S. 47–94.
- D. J. McGarvey, R. Croteau: Terpenoid metabolism. In: Plant Cell. Band 7, Nr. 7, Juli 1995, S. 1015–1026, doi:10.1105/tpc.7.7.1015, PMID 7640522, PMC 160903 (freier Volltext).
- J. D. Newman, J. Chappell: Isoprenoid biosynthesis in plants: carbon partitioning within the cytoplasmic pathway. In: Crit. Rev. Biochem. Mol. Biol. Band 34, Nr. 2, 1999, S. 95–106, doi:10.1080/10409239991209228, PMID 10333387.
Einzelnachweise
- MetaCyc: mevalonate pathway I
- MetaCyc: mevalonate pathway II (archaea)