Methylerythritolphosphatweg
Der Methylerythritolphosphatweg, auch MEP-Weg oder DOXP-Weg, ist ein Stoffwechselweg, der zur Synthese von Dimethylallylpyrophosphat (DMAPP) und Isopentenylpyrophosphat (IPP), zwei Isoprenen, führt. Er kommt in den Plastiden der Pflanzen,[1] verschiedenen Protozoen,[2] Bakterien und Algen vor und wurde auch für den einzelligen Parasiten Plasmodium falciparum beschrieben.[3][4] In vielen höher entwickelten Eukaryoten und manchen Bakterien findet die Synthese dieser Isoprene im sogenannten Mevalonatbiosyntheseweg statt.
| Übergeordnet |
| Phospholipid-Biosynthese |
| Gene Ontology |
|---|
| QuickGO |
Der Methylerithritolphosphatweg wurde durch die Forschergruppen um Michel Rohmer und Duilio Arigoni entdeckt.[5] In der englischsprachigen Literatur wird er unter non-mevalonate pathway geführt.
Biochemie
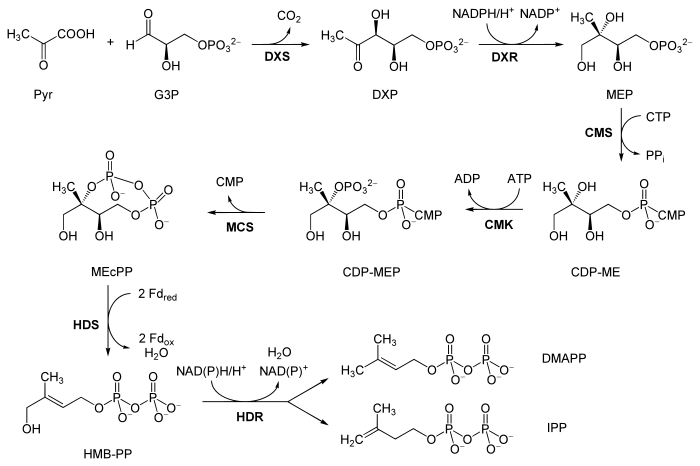
Der Stoffwechselweg beginnt mit der Verknüpfung von Pyruvat und Glycerinaldehyd-3-phosphat (G3P). Diese Reaktion katalysiert eine Desoxyxylulosephosphat-Synthase (DXS, EC 2.2.1.7) unter Kohlenstoffdioxidabspaltung, wobei 1-Desoxy-D-xylulose-5-phosphat (DXP) entsteht. DXP ist außerdem der Vorläufer für die Pyridoxal- und Thiaminbiosynthese.
DXP wird durch die DXP-Reduktoisomerase (DXR, EC 1.1.1.267) reduziert und zu 2C-Methyl-D-erythritol-4-phosphat (MEP) isomerisiert, wobei NADPH zu NADP+ oxidiert wird. An MEP wird dann Cytidindiphosphat (CDP) angeknüpft, was eine Cytidindiphosphat-Methylerythritol-Synthase (CMS, EC 4.6.1.12) katalysiert. Bei dieser Reaktion wird Cytidintriphosphat (CTP) verbraucht und Pyrophosphat (PPi) abgespalten. Das entstandene Produkt, 4-Diphosphocytidyl-2C-methyl-D-erythritol (CDP-ME), wird unter Adenosintriphosphat (ATP)-Verbrauch zu 4-Diphosphocytidyl-2C-methyl-D-erythritol-2-P (CDP-MEP) phosphoryliert, was eine Cytidyl-Methyl-Kinase (CMK, EC 2.7.1.148) katalysiert.
Die nun folgende Reaktion ist eine Zyklisierung, bei der unter Abspaltung von Cytidinmonophosphat (CMP) ein Phosphorsäureester zwischen C2 und C4 entsteht. Die Reaktion wird durch die Methyl-Erythritol-Cyclo-Diphosphat-Synthase (MCS, EC 4.6.1.12) katalysiert, es entsteht 2C-Methyl-D-erythritol-2,4-cyclodiphosphat (MEcPP). Die Hydroxy-Methyl-Butenyl-Diphosphat-Synthase (HDS, EC 1.17.7.1) katalysiert dann die Umsetzung zu (E)-4-Hydroxy-3-methylbut-2-enyldiphosphat (HMB-PP) und Wasser, wobei zwei reduzierte Ferredoxine als Reduktionsmittel fungieren. Das nun folgende Enzym katalysiert sowohl die Umsetzung zu IPP wie auch DMAPP in einem Verhältnis von 5:1. Das hierfür verantwortliche Enzym ist die IPP/DMAPP-Synthase (IDS, EC 1.17.1.2), es wird NAD(P)H oxidiert und Wasser abgespalten.
Pharmakologie
Dieser Stoffwechselweg findet in Plasmodium falciparum, dem Erreger der Malaria, statt. Daher ist er auch ein Angriffspunkt für die Entwicklung von Pharmazeutika gegen Malaria geworden. Das bekannteste Medikament, das blockierend gegen den MEP-Weg wirkt, ist das Fosmidomycin.[6][7]
Einzelnachweise
- E. Cordoba, M. Salmi, P. León: Unravelling the regulatory mechanisms that modulate the MEP pathway in higher plants. In: Journal of experimental botany. Band 60, Nummer 10, 2009, S. 2933–2943, doi:10.1093/jxb/erp190. PMID 19584121.
- S. N. Moreno, Z. H. Li: Anti-infectives targeting the isoprenoid pathway of Toxoplasma gondii. In: Expert Opinion on Therapeutic Targets. Band 12, Nummer 3, März 2008, S. 253–263, doi:10.1517/14728222.12.3.253. PMID 18269336.
- Lichtenthaler, H. (1999): The 1-Deoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants. In: Annu Rev Plant Physiol Plant Mol Biol 50; 47–65; PMID 15012203; doi:10.1146/annurev.arplant.50.1.47
- Rohmer, M. (1999): The discovery of a mevalonate-independent pathway for isoprenoid biosynthesis in bacteria, algae and higher plants. In: Nat Prod Rep, 16(5); 565–574; PMID 10584331; doi:10.1039/a709175c
- Rohdich, F. et al. (2002): Studies on the nonmevalonate terpene biosynthetic pathway: Metabolic role of IspH (LytB) protein. In: Proc Natl Acad Sci USA 99(3); 1158–1163; PMID 11818558; PDF
- Chemistry & Biology, (1998), 5, 221–233 und Annual Review of Plant Physiology and Plant Molecular biology, (1999), 50, 47–65.
- Jomaa H. et al. (1999): Inhibitors of the nonmevalonate pathway of isoprenoid biosynthesis as antimalarial drugs. In: Science, 285(5433); 1573–1576; PMID 10477522; doi:10.1126/science.285.5433.1573