Mannose-bindendes Lektin
Das Mannose-bindende Lektin (MBL) ist ein Protein des angeborenen Immunsystems in Säugetieren. Beim Menschen wird das Protein in der Leber als Reaktion auf eine Infektion produziert und ins Blut ausgeschüttet.[2] Mutationen im MBL2-Gen können zu MBL-Mangel führen, der mit erhöhter Infektionsanfälligkeit assoziiert ist.[3]
| Mannose-bindendes Lektin | ||
|---|---|---|
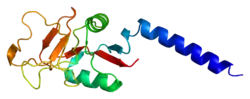 | ||
| Bändermodell der Aminosäuren 108-248 im Monomer des Mannose-bindenden Lektins | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 228 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Oligomer aus Homotrimeren | |
| Kofaktor | Ca2+ | |
| Bezeichner | ||
| Gen-Name | MBL2 | |
| Externe IDs | ||
| Vorkommen | ||
| Übergeordnetes Taxon | Säugetiere[1] | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 4153 | 17195 |
| Ensembl | ENSG00000165471 | ENSMUSG00000024863 |
| UniProt | P11226 | P41317 |
| Refseq (mRNA) | NM_000242 | NM_010776 |
| Refseq (Protein) | NP_000233 | NP_034906 |
| Genlocus | Chr 10: 52.76 – 52.77 Mb | Chr 19: 30.23 – 30.24 Mb |
| PubMed-Suche | 4153 | 17195 |
MBL ist Mitglied der Akute-Phase-Proteine und ein Collectin. Collectine gehören zur Obergruppe der C-Typ Lektin-Rezeptoren, deren Aufgabe die Erkennung fremder Strukturen als erste Stufe der Immunabwehr ist. MBL erkennt hierbei Kohlenhydrat-Muster, die sich auf der Oberfläche einer großen Anzahl von pathogenen Mikroorganismen, unter anderem Bakterien, Viren, Protozoen und Pilze befinden. Wenn das MBL an einen Mikroorganismus bindet, folgt die Aktivierung des Komplementsystems über den Lektin-Weg.[4][5][6]
Struktur
MBL hat eine oligomere Struktur (400–700 kDa) und besteht aus mehreren Untereinheiten, die jeweils drei identische Peptidketten von etwa 32 kDa Größe enthalten. Obwohl es verschiedene oligomere Formen bilden kann, gibt es Hinweise darauf, dass Dimere und Trimere nicht biologisch aktiv sind und mindestens eine tetramere Form notwendig ist, um das Komplementsystem zu aktivieren.[7]
Das Mannose-bindende Lektin weist dabei alle wichtigen Strukturmerkmale der Collectin-Proteine auf: Es hat zwei bis sechs Cluster mit CRDs (carbohydrate recognition domains).[8] In jedem der Cluster befinden sich die Kohlenhydrat-Bindestellen an einem festen Ort, was die Grundlage für die spezifischen Erkennung darstellt. Außerdem weist das Protein noch eine Kollagen-Tripelhelix als Bindestelle für Proteine, eine gewundene α-helikale Coiled-Coil-Struktur, als Verbindungsstück zwischen Kohlenhydrat- und Protein-Bindestelle und eine N-terminale cysteinreiche Domäne auf.[9] Im Blut bildet MBL mit den Serinproteasen MASP-1 und MASP-2 (MBL-associated serine protease) einen Proteinkomplex. Dieser ähnelt dem C1-Komplex des klassischen Wegs stark, sodass davon ausgegangen wird, dass beide den gleichen evolutionären Ursprung haben.[10]
Wirkungsweise
Das Komplementsystem kann über drei verschiedene Wege aktiviert werden: den klassischen Weg, den alternativen Weg und den Lektin-Weg. Das Mannose- bindende Lektin nutzt den sog. Lektin-Weg.[11] Hierbei bindet es an Mannose oder N-Acetylglucosamin auf der pathogenen Oberfläche (z. B. bakterielles Peptidoglykan) und aktiviert dann die MBL-aktivierten Proteasen MASP-1, MASP-2 und MASP-3. Die MASP-2 Proteine spalten die Blutproteine C4 und C2 in jeweils zwei Fragmente: C4a, C4b, C2a, C2b. Die Rolle der anderen MASP-Proteine ist nicht endgültig geklärt, sie scheinen allerdings die Aufspaltung zu verstärken, auch wenn sie sie nicht selbst initiieren können.[12]
Die C4b- und C2b-Fragmente verknüpfen sich dann auf der Membranoberfläche des Pathogens und führen zur Bildung einer C3-Konvertase. Die darauffolgende Komplementkaskade gleicht dem klassischen Weg. Sie wird durch die C3-Konvertase katalysiert und führt zur Bildung eines Membranangriffskomplexes (MAC). Schlussendlich erfolgt die Lyse des an das MBL gebundenen Krankheitserregers. MBL bindet nachgewiesenermaßen an Hefen, wie Candida albicans,[13] an Viren wie HIV[14] und Influenza A, an viele Bakterien, unter anderem Salmonellen und Streptokokken und an Parasiten wie Leishmanien.[15]
Mutationen
Das MBL2-Gen codiert für das Mannose-bindende Lektin, das von der Leber in den Blutkreislauf gebracht wird. Auch wenn die Konzentration des MBLs im menschlichen Serum relativ gering ist (1500 Mikrogramm/Liter), nimmt MBL eine entscheidende Rolle bei der angeborenen Immunabwehr ein.[16] Die Häufigkeit eines mutationsbedingten Immundefekts, der zu einem Mangel an Mannose-bindenden Lektin führt, wird auf 5 bis 10 % geschätzt.[17] Eine solche Mangelerscheinung führt zu einem erhöhten Krankheitsrisiko; nicht nur die Häufigkeit, sondern auch die Schwere der Krankheitsverläufe nimmt zu. Obwohl die meisten Menschen mit MBL-Mangel gesund sind, haben sie eine erhöhte Anfälligkeit für bestimmte Krankheiten.[18] Die Mangelkrankheit ist dabei bei Kleinkindern mit wiederkehrenden Atemwegserkrankungen, Mittelohrentzündungen und chronischer Diarrhöe besonders häufig. Die meist niedrige Konzentration von MBL in Kleinkindern mit wiederholten Infektionenskrankheien, legt nahe, dass der Mannose Bindende-Lektin-Weg in dem Zeitraum zwischen dem Verlust der passiv erhaltenen Antikörper der Mutter und der Bildung eines eigenen ausgereiften immunologischen Abwehrsystems, eine wichtige Rolle spielt.[19]
Obwohl die eigentliche Aufgabe von MBL darin besteht, Bakterien und andere Krankheitserreger zu eliminieren, führt ein MBL-Mangel auch zu autoimmunen Krankheitsbildern wie Lupus erythematodes und rheumatische Arthritis. Das Immunsystem weist viele überzählige Reaktionswege auf, damit es weiter funktionsfähig bleibt, falls einer der Wege nicht funktioniert. In unserem Fall führen der klassische, der Lektin- und der alternative Weg zur C3-Konvertase und über diese gemeinsame Zwischenstufe zur Aktivierung des Komplementsystems. Wenn der MB-Lektin-Weg aufgrund des MBL-Mangels nicht ausreichend gut funktioniert, wird dies vom Immunsystem durch die entsprechende Verstärkung der anderen Komplementkaskaden ausgeglichen. Besonders nennenswert ist dabei die Zunahme der Konzentration der Antikörper, die als Ausgangsprodukt des klassischen Wegs gebraucht werden. Die stark erhöhte Anzahl an sich im Umlauf befindlichen Antikörpern erhöht proportional das Erkrankungsrisiko von rheumatischer Arthritis.[20]
Therapiemöglichkeiten
Die Therapie eines MBL-Mangels ist ein Gebiet der aktuellen Forschung. Diese beinhaltet die intravenöse Infusion von reinem, aus menschlichem Spenderblut gewonnenen MBL mit dem Ziel Infektionen zu verhindern oder abzuschwächen. Die MBL-Therapie könnte in Zukunft in drei klinischen Situationen eingesetzt werden: Erstens könnte der MBL-Ersatz dazu genutzt werden die Immunabwehr gegenüber Krankheiten zu stärken. Zweitens, im Falle einer akuten Infektion, könnte die MBL-Therapie den Krankheitsverlauf abschwächen und zu schnellerer Heilung führen. Jedoch zeigen Analogien mit ähnlichen Mangelerscheinungen, dass der MBL-Ersatz mehr schaden als nützen könnte, da er zu größeren Schäden im Wirtsorganismus führt. Außerdem könnte die MBL-Therapie zur Veränderung des Verlaufs chronischer Krankheiten genutzt werden.[21]
Weblinks
- de Bono / reactome: Lectin pathway of complement activation
Einzelnachweise
- Orthologe bei OMA
- E. Tutdibi, A. Schwarz, D. Monz, G. Dockter, L. Gortner: Surfactantprotein D und Mannose-bindendes Lektin im Serum bei Patienten mit CF und chronischer Pseudomonas aeruginosa Infektion. In: Z Geburtshilfe Neonatol. Band 213, 2009. doi:10.1055/s-0029-1223124.
- UniProt P11226
- I. P. Fraser, H. Koziel, R. A. Ezekowitz: The serum mannose-binding protein and the macrophage mannose receptor are pattern recognition molecules that link innate and adaptive immunity.. In: Semin. Immunol.. 10, Nr. 5, 1998, S. 363–72. doi:10.1006/smim.1998.0141. PMID 9799711.
- Worthley DL, Bardy PG, Mullighan CG: Mannose-binding lectin: biology and clinical implications.. In: Internal medicine journal. 35, Nr. 9, 2005, S. 548–55. doi:10.1111/j.1445-5994.2005.00908.x. PMID 16105157.
- Worthley DL, Bardy PG, Gordon DL, Mullighan CG: Mannose-binding lectin and maladies of the bowel and liver. In: World J. Gastroenterol.. 12, Nr. 40, Oktober 2006, S. 6420–8. PMID 17072973.
- S. Sheriff, C. Y. Chang, R. A. Ezekowitz: Human mannose-binding protein carbohydrate recognition domain trimerizes through a triple alpha-helical coiled-coil. In: Nat. Struct. Biol.. 1, Nr. 11, November 1994, S. 789–94. doi:10.1038/nsb1194-789. PMID 7634089.
- Janeway et al.: Immunobiology. Garland Science, New York, NY. 2005, S. 54–55.
- Misao Matsushita et al.: Proteolytic activities of two types of mannose-binding lectin-associated serine protease. In: The Journal of Immunology. Band 165, 2000, S. 2637–2642.
- Janeway et al.: Immunobiology. Garland Science, New York, NY. 2005, S. 66–67.
- Lauren Sompayrac: How the Immune System Works. Blackwell Science, Malden, MA. 1999, S. 17–19.
- Janeway et al.: Immunobiology. Garland Science, New York, NY. 2005, S. 66.
- M. A. de Jong, L. E. Vriend, B. Theelen, M. E. Taylor, D. Fluitsma, T. Boekhout, T. B. Geijtenbeek: C-type lectin Langerin is a beta-glucan receptor on human Langerhans cells that recognizes opportunistic and pathogenic fungi. In: Mol. Immunol.. 47, Nr. 6, März 2010, S. 1216–1225. doi:10.1016/j.molimm.2009.12.016. PMID 20097424. PMC 2837148 (freier Volltext).
- X. Ji, H. Gewurz, G. T. Spear: Mannose binding lectin (MBL) and HIV. In: Mol. Immunol.. 42, Nr. 2, Februar 2005, S. 145–152. doi:10.1016/j.molimm.2004.06.015. PMID 15488604.
- Lauren Sompayrac: How the Immune System Works. Blackwell Science, Malden, MA. 1999, S. 17–19.
- M. W. Turner: Mannose-binding lectin (MBL) in health and disease. In: Immunobiology. Band 199. Nr. 2, 1998, S. 327–339.
- M. W. Turner: Deficiency of mannan binding protein--a new complement deficiency syndrome. In: Clin Exp Immunology Band 86, 1991, S. 53–56.
- Flemming et al.: Disease-associated mutations in human mannose-binding lectin compromise oligomerization and activity of the final protein. In: Journal of Biological Chemistry. Band 279, 2004, S. 21302–21311.
- Summerfield et al.: Association of mutations in mannose binding protein gene with childhood infection in consecutive hospital series. In: British Medical Journal Band 314, 1997, S. 1229–1231.
- S. Jacobsen et al.: The influence of mannose binding lectin polymorphisms on disease outcome in early polyarthritis. In: The Journal of Rheumatology. Band 28, Nr. 5, 2001, S. 935–942.
- J. A. Summerfiled: Clinical potential of mannose-binding lectin-replacement therapy. In: Biochemical Society Transactions. Aug. 2003, S. 770–773.