Mangan(III)-acetylacetonat
Mangan(III)-acetylacetonat (Mn(acac)3) ist ein Komplex des Mangans der Oxidationsstufe +3, mit Acetylacetonat als Ligand.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
-acetylacetonat.svg.png.webp) | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Mangan(III)-acetylacetonat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C15H21MnO6 | ||||||||||||||||||
| Kurzbeschreibung |
schwarzer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 352,3 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt |
159–161 °C (Zersetzung)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Mangan(III)-acetylacetonat wird aus einem Mangan(II)-Salz, Kaliumpermanganat und Acetylaceton hergestellt.
Bei der Reaktion entsteht zunächst als Zwischenprodukt Mangan(II)-acetylacetonat:
Durch die Reaktion von Mn(II) und Mn(VII) entsteht Mn(III):
Gesamtreaktion:
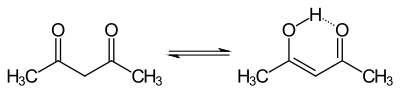
Durch Zugabe von Natriumacetat wird die entstehende Säure gepuffert. Des Weiteren sorgt es für die Verschiebung des Gleichgewichtes in der Enol-Keto-Tautomerie des Acetylaceton.
Durch die schwach basische Eigenschaft des Natriumacetats wird die Enol-Form deprotoniert und das Acetylaceton in seine Anionische Form überführt. Somit stabilisiert es das d4-Konfigurierte Mangan-Ion durch Komplexbildung.
Eigenschaften
-acetylacetonat.JPG.webp)
Mangan(III)-acetylacetonat ist ein schwarzes, kristallines, in Wasser unlösliches Pulver. Der elektronischen Struktur nach, bildet es einen High Spin-Komplex aus.[2] Die Struktur ist aufgrund des Jahn-Teller-Effektes oktaedrisch verzerrt. Dieser kann entweder oktaedrisch-gestaucht oder oktaedrisch-gestreckt sein. Bei der Streckung, betragen die Längen zweier Mn-O-Bindungen 2,12 Å, wobei die vier anderen nur 1,93 Å betragen. Bei der Kompression, betragen die Längen zweier Mn-O Bindungen 1,95 Å, während die anderen vier Bindungslängen 2,00 Å betragen.
Verwendung
Mangan(III)-acetylacetonat wird zur Oxidation von Phenolen, β-Dicarbonylverbindungen und Thiolen verwendet.[1]
Literatur
- J. Derek Woollins: Inorganic Experiments. Wiley-VCH, Weinheim 1994, ISBN 3-527-29253-5, S. 118–119.
- F. Albert Cotton, Geoffrey Wilkinson, Carlos A. Murillo, Manfred Bochmann: Advanced Inorganic Chemistry. 6th ed. Wiley-Interscience, New York 1999, ISBN 0-471-19957-5.
Einzelnachweise
- Datenblatt Manganese(III) acetylacetonate bei Sigma-Aldrich, abgerufen am 18. Juni 2012 (PDF).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1616–1617.