Lithiumnitrat
Lithiumnitrat ist eine chemische Verbindung mit der Summenformel LiNO3, die natürlich in der Form des Trihydrates LiNO3·3 H2O vorkommt. Es handelt sich hierbei um das Lithiumsalz der Salpetersäure.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
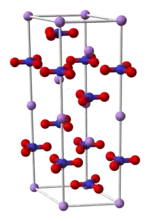 | ||||||||||||||||
| _ Li+ _ N3+ _ O2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Lithiumnitrat | |||||||||||||||
| Verhältnisformel | LiNO3 | |||||||||||||||
| Kurzbeschreibung |
farbloser, zerfließlicher Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 68,95 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
2,36 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
Zersetzung > 600 °C[2] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Die Herstellung von Lithiumnitrat erfolgt durch Umsetzung von Lithiumcarbonat[5] oder Lithiumhydroxid[6] mit Salpetersäure.
Eigenschaften

Das farblose, hygroskopische Salz besitzt eine Molare Masse von 68,95 g/mol, eine Dichte von 2,36 g·cm−3 und eine Schmelztemperatur von 264 °C. Bei Temperaturen oberhalb von 600 °C erfolgt Zersetzung. Lithiumnitrat ist in Ethanol und Wasser sehr gut löslich. Neben der wasserfreien Kristallform tritt Lithiumnitrat auch als Trihydrat auf, welches bei 28,8 °C[7] sein Kristallwasser abgibt. Unterkühlte Schmelzen des Hydrats sind sehr stabil, können aber durch Zugabe von kristallinem Lithiumnitrat augenblicklich zur Kristallisation gebracht werden.
Verwendung
Entgegen der weit verbreiteten Auffassung[5] wird LiNO3 nicht für rote Leucht- oder Signalsätze verwendet. Bei den für pyrotechnische Leuchtsätze typischen Flammentemperaturen erfolgt immer auch eine starke Anregung der Li-Nebenserienlinien, wodurch ein insgesamt rot-oranger Farbeindruck entsteht, welcher aber einfacher durch die Verwendung von Calciumsalzen erreicht werden kann[8]. Lithiumnitrat wird als Wärmeträgermedium[9] genutzt. Des Weiteren kann es zur Herstellung anderer Lithiumverbindungen dienen. Lithiumnitrat wird auch in einem Gemisch mit Kaliumnitrat als Sabalith verkauft. Dieses niedrigschmelzende Eutektikum wird zur Salzbadvulkanisation von Gummimischungen verwendet.[10] Lithiumnitrat-trihydrat wurde auch zur Kühlung des Landers der Venera-Mission verwendet, da es beim Schmelzen (Schmelzpunkt des Trihydrats ca. 30 °C) Wärme aufnimmt und somit bis zum vollständigen Schmelzen eine kontinuierliche Temperatur von 30 °C gewährleistet.[11]
Einzelnachweise
- Eintrag zu Lithiumnitrat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. Juli 2014.
- Datenblatt Lithiumnitrat (PDF) bei Merck, abgerufen am 19. Januar 2011.
- Eintrag zu Lithiumnitrat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Datenblatt Lithium nitrate bei Sigma-Aldrich, abgerufen am 8. April 2011 (PDF).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 1154.
- D. L. Perry, S. L. Phillips: Handbook of Inorganic Compounds: An Electronic Database. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 228.
- A. N. Campbell: The Systems: LiNO3-NH4NO3 and LiNO3-NH4NO3-H2O. In: Journal of the American Chemical Society. 64, 1942, S. 2680–2684, doi:10.1021/ja01263a043.
- E.-C. Koch: Evaluation of Lithium Compounds as Color Agents for Pyrotechnic Flames. In: J. Pyrotech 13, 2001, 1. (Abstract).
- Europäisches Patent EP0363678, 1989, Metzler GmbH.
- Winnacker, Küchler: Chemische Technik: Prozesse und Produkte. (PDF; 2,3 MB) 2006, Wiley-VCH Weinheim, ISBN 3-527-31578-0.
- www.Bernd-leitenberger.de.

