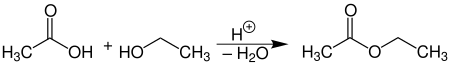Ethylester
Ethylester sind chemische Verbindungen, die zur Gruppe der Ester gehören. Sie entstehen durch Veresterung einer Carbonsäure oder einer anorganischen Oxosäure mit Ethanol und weisen die charakteristische funktionelle Estergruppe auf. Neben den Carbonsäureestern zählen zu den Ethylestern auch Kohlensäureester und Ester, die sich von Sulfonsäuren und Ethanol ableiten. Analog können sich auch aus Salpetersäure, Sulfinsäuren, Phosphonsäuren oder Phosphinsäuren einerseits und Ethanol andererseits Ethylester bilden. Orthoameisensäuretriethylester, HC(OC2H5)3, ist ein bekannter Vertreter der Orthocarbonsäureester.[1]
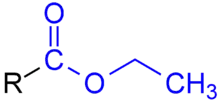
ethylester ist R ein Chloratom.
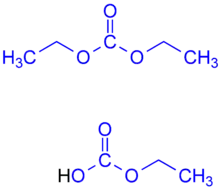
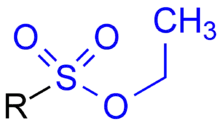
Vorkommen
Carbonsäureethylester kommen als sogn. Fruchtester in vielen Früchten und Speisen als geruchsgebende Komponente vor. In der Natur kommt Buttersäureethylester in verschiedenen Pflanzen vor, z. B. in Erdbeeren, Äpfeln, Orangen und Ananas. (Z)-4-Decensäureethylester, (E)-2-Octensäureethylester und (E,Z)-2,4-Decadiensäureethylester findet man in Birnen, (S)-2-Methylbuttersäureethylester in Orange und Ananas. Ethylformiat ist ein Bestandteil von Rum und Arrak.[2]
Herstellung
Ethylester entstehen z. B. aus einer Carbonsäure und Ethanol unter säurekatalysierter Wasserabspaltung.
Aus Carbonsäurechloriden und Ethanol können nach der Schotten-Baumann-Methode ebenfalls Ethylester erhalten werden. Ethylester lassen sich auch aus Carbonsäureanhydriden und Ethanol synthetisieren. Die nucleophile Substitution von Methylhalogeniden (z. B. Ethyliodid) mit Carboxylat-Ionen liefert auch Ethylester.
Entsprechend bilden sich Diethylester aus Dicarbonsäuren und Ethanol, Triethylester aus Tricarbonsäuren und Ethanol usw.
Verwendung
Essigsäureethylester wird als Lösungs- und Gelatinierungsmittel – z. B. für Kollodiumwolle und Celluloid – in der Industrie eingesetzt. Einige Ethylester von Carbonsäuren werden als Geschmacks- und Aromastoffe benutzt.
Ethylester können durch ihre erhöhte Lipophilie Barrieren passieren bzw. Aminosäuretransportdefekte umgehen. Ethylester von L-Tryptophan und eventuell weiterer Aminosäuren sind die einzige Behandlungsmöglichkeit für schwere Fälle der Hartnup-Krankheit.[3]
Siehe auch
- Methylester, Carbonsäureester, die sich vom Methanol ableiten
Einzelnachweise
- Siegfried Hauptmann: Organische Chemie, 2. durchgesehene Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, ISBN 3-342-00280-8, S. 421.
- Wolfgang Legrum: Riechstoffe, zwischen Gestank und Duft, Vieweg + Teubner Verlag (2011), ISBN 978-3-8348-1245-2, S. 85–86.
- A. J. Jonas, I. J. Butler: Circumvention of defective neutral amino acid transport in Hartnup disease using tryptophan ethyl ester. In: The Journal of clinical investigation. Band 84, Nummer 1, Juli 1989, S. 200–204, ISSN 0021-9738. doi:10.1172/JCI114141. PMID 2472426. PMC 303970 (freier Volltext).