Elvucitabin
Elvucitabin (ACH-126,443) ist ein experimenteller Arzneistoff zur Behandlung von HIV-infizierten Patienten im Rahmen einer HIV-Kombinationstherapie, sowie einer HBV-Infektion.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
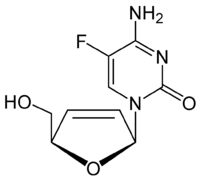 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Elvucitabin | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | C9H10FN3O3 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| Wirkstoffklasse |
Virostatikum, nukleosidische Reverse-Transkriptase-Inhibitoren | |||||||||||||||
| Wirkmechanismus | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 227,19 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Elvucitabin ist ein Cytidinanalogon und gehört zur Gruppe der nukelosidischen Reverse-Transkriptase-Inhibitoren (NRTI).
Geschichte
Elvucitabin wurde von Achillion Pharmaceuticals entwickelt. Eine Studie mit Patienten mit Lamivudin (Epivir) oder Emtricitabin (Emtriva) Resistenz und gleichzeitiger M184 Mutation wurde 2007 beendet. Derzeit ist unklar, ob die Substanz überhaupt noch weiter entwickelt wird.[2] Die letzte Veröffentlichung ist von 2011.[3][4]
Pharmakologie
Elvucitabin ist ein Enantiomer von Dexelvucitabin (Reverse) und besitzt ebenfalls eine Wirksamkeit gegen HIV und HBV. Derzeit laufen Phase II-Studien bei HIV und HBV. Bei HIV-Patienten mit der M184V-Mutation zeigte sich in einer kleinen, doppelblinden Studie ein Abfall der Viruslast um 0,7–0,8 Logstufen nach 28 Tagen. Die Studie wurde allerdings abgebrochen, da unter 100 mg Elvucitabine bei 6/56 Patienten Leukopenien auftraten.[5]
Vergleichsstudien mit Epivir lassen vermuten, dass die suppressive Wirkung von Elvucitabin geringfügig schwächer ist (durchschnittlich 0,3 Logstufen).[2]
Die mitochondriale Toxizität scheint geringer als unter Dexelvucitabine. Derzeitige Ergebnisse zeigen, dass möglicherweise auch die Bindungsaffinität zur Reversen Transkriptase resistenter Viren geringer ist.[6]
Pharmakokinetik
In Studien wurde eine extrem lange Halbwertszeit von 150 Stunden ermittelt.[7] Vor diesem Hintergrund scheint eine einmal tägliche Gabe sehr wahrscheinlich.
Nebenwirkungen
Positiv fiel in Studien die offenbar geringe mitochondriale Toxizität auf.[8] Eine Studie musste allerdings abgebrochen werden, da unter 100 mg Elvucitabine bei 6/56 Patienten Leukopenien auftraten.[5] Einige Patienten entwickelten außerdem Hautausschläge. Pankreatitiden wie unter Dexelvucitabine scheinen dagegen nicht aufzutreten.
Resistenzen
In-vitro zeigte sich eine gute Wirksamkeit gegen verschiedene NRTI-Resistenzen. Es wurde die Selektion von Viren mit ganz eigenen Resistenzen wie M184I oder die bislang ganz unbekannte Mutante D237E beobachtet.[9] Wahrscheinlich wird die Selektion dieser speziellen Resistenzen unter HAART nicht zu beobachten sein.[2]
Einzelnachweise
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Eintrag Elvucitabine (Memento des Originals vom 21. März 2008 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. auf aidsmeds.com.
- R. K. Ghosh, S. M. Ghosh, S. Chawla: Recent advances in antiretroviral drugs. In: Expert opinion on pharmacotherapy. Band 12, Nummer 1, Januar 2011, S. 31–46, doi:10.1517/14656566.2010.509345, PMID 20698725.
- M. Desai, G. Iyer, R. K. Dikshit: Antiretroviral drugs: critical issues and recent advances. In: Indian journal of pharmacology. Band 44, Nummer 3, Mai 2012, S. 288–298, doi:10.4103/0253-7613.96296, PMID 22701234, PMC 3371447 (freier Volltext).
- Dunkle LM. et al. (2003): Elvucitabine: potent antiviral activity demonstrated in multidrug-resistant HIV infection. In: Antiviral Therapy 8:S5.
- Murakami E. et al. (2004): Investigating the effects of stereochemistry on incorporation and removal of 5-fluorocytidine analogs by mitochondrial DNA polymerase gamma: comparison of D- and L-D4FC-TP. In: Antiviral Res. 62 (1); 57–64, PMID 15026203.
- Colucci P, Pottage J, Robison H, et al. The different clinical pharmacology of elvucitabine (beta-L-Fd4C) enables the drug to be given in a safe and effective manner with innovative drug dosing. Abstract LB-27, 45th ICAAC 2005, Washington.
- Dunkle LM, Oshana1 SC, Cheng YC, et al.: ACH-126,443: a new nucleoside analog with potent activity against wild type and resistant HIV-1 and a promising pharmacokinetic and mitochondrial safety profile (Memento des Originals vom 21. August 2009 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.. Abstract 303, 8th CROI 2001, Chicago.
- Fabrycki J. et al. (2003): In vitro induction of HIV variants with reduced susceptibility to elvucitabine (ACH-126,443,beta-L-Fd4C). Antiviral Therapy 8:S8.