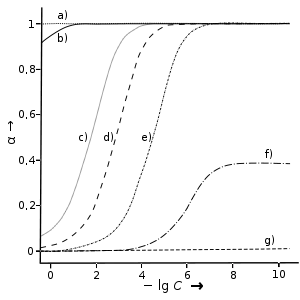
Dissoziationsgrad
Der dimensionslose Dissoziationsgrad α (auch Protolysegrad genannt) gibt das Verhältnis der dissoziierten Säure- bzw. Base-Teilchen zur formalen Anfangskonzentration der undissoziierten Säure bzw. Base in einer wässrigen Lösung an. Der Dissoziationsgrad einer Säure bzw. Base hängt von ihrer Säurekonstante (bzw. Basenkonstante), ihrer Konzentration und dem vorliegenden pH-Wert einer Lösung ab. Liegt in einer Lösung nur eine Säure oder Base vor, lässt sich der Dissoziationsgrad aus der elektrolytischen Leitfähigkeit der Lösung experimentell bestimmen. Ist der pH-Wert einer Lösung bekannt, lässt sich der Dissoziationsgrad rechnerisch abschätzen.
Der Dissoziationsgrad kann Werte zwischen 0 und 1 annehmen.
Einprotonige Säuren HA
Für eine einprotonige Säure HA mit der formalen Ausgangskonzentration c0, die dissoziiert gemäß der Gleichung
gilt:
gibt also den relativen Anteil an dissoziierter Säure an, c0 die Anfangskonzentration der undissoziierten Säure.
Die Definition eines Dissoziationsgrades für Basen ist nicht eigens erforderlich, da er bereits in enthalten ist.
Der Assoziationsgrad („degree of formation“) der relative Anteil an nicht dissoziierter Säure, ergibt sich aus:
Die Kombination des Massenwirkungsgesetzes für das Protolysegleichgewicht
(KS ist die Säurekonstante, die als Maß für die Säurestärke gilt)
mit der Massenerhaltung der Säure in der Lösung
führt zu folgendem Ausdruck für den Dissoziationsgrad:
Die Gleichung zeigt, dass der Dissoziationsgrad einer bestimmten Säure mit bekanntem pKs-Wert nur vom pH-Wert der Lösung abhängt. Sie lässt sich umformen zu:
d. h. der pH-Wert einer solchen Lösung ist selbst eine Funktion der Gesamtkonzentration c0 der Säure.
Zweiprotonige Säuren H2A
Bei zwei oder mehrprotonigen Säuren ist es zweckmäßig, auf die Unterscheidung zwischen Dissoziationsgrad und Assoziationsgrad zu verzichten. Stattdessen definiert man allgemein den Anteil an der formalen Ausgangskonzentration c0 der Säure, der auf eine der in Lösung vorliegenden Spezies entfällt. Die Verteilung auf die verschiedenen Formen hängt dabei vom pH-Wert der Lösung ab.
Eine zweiprotonige Säure dissoziiert in wässriger Lösung in zwei Gleichgewichtsreaktionen:
Die Gleichgewichte werden durch die zwei Säuredissoziationskonstanten beschrieben:
Die bei gegebenem pH-Wert auf die verschiedenen Säurespezies entfallenden Anteile berechnen sich dann gemäß:
mit der Hilfsvariablen
Titrationskurven lassen sich erhalten, indem man den (verallgemeinerten) Assoziationsgrad als Funktion des pH-Wertes aufträgt. Der analoge Dissoziationsgrad ist dann gegeben durch . Analog geht man im Fall einer mehrprotonigen Säure vor.[1]
Mehrprotonige Säuren HnA
Eine mehrprotonige Säure HnA unterliegt in Lösung n gekoppelten Protolysegleichgewichten, beschrieben durch die Säuredissoziationskonstanten . Bei gegebenem pH-Wert berechnet sich der auf die Spezies entfallende Anteil gemäß:
In allen Fällen gilt stets: .
Analog zum Fall der zweiprotonigen Säure ist der Assoziationsgrad für die n-protonigen Säure durch gegeben.
Konduktometrische Bestimmung
Bei Säuren mit einem Wasserstoffatom lässt sich der Dissoziationsgrad über konduktometrische Messungen bestimmen nach der Formel:
mit
Eine ähnliche Bestimmung ist auch für Säuren mit mehreren Wasserstoffatomen oder auch mit Salzen möglich (Aktivität (Chemie)).
Einzelnachweise
- James Newton Butler: Ionic Equilibrium: Solubility and PH Calculations. John Wiley & Sons, 1998, ISBN 978-0-471-58526-8, S. 185 ff..