Chlordecon
Chlordecon ist eine chemische Verbindung aus der Gruppe der Organochlorverbindungen und Ketone. Technisch reines Chlordecon enthält etwa 5 % Wasser und bis zu 0,1 % Hexachlorcyclopentadien.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
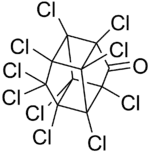 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Chlordecon | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C10Cl10O | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 490,64 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser (2–4 mg·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
Chlordecon kann durch Dimerisierung von Hexachlorcyclopentadien und nachfolgender Hydrolyse zu einem Keton dargestellt werden.[4]
Eigenschaften
Chlordecon ist in der Umwelt sehr stabil mit einer Halbwertszeit von mehreren Jahrzehnten in Böden.[5]
Verwendung
Chlordecon wurde als Insektizid und als Zwischenprodukt zur Herstellung des Insektizids Kelevan verwendet. Es wurde 1958 unter dem Namen Kepone als Ketonanalogon von Mirex eingeführt und zwischen 1966 und 1975 in den USA als Insektizid gegen Ameisen und Kakerlaken eingesetzt.[6] 1975 wurde der Einsatz in den USA verboten, und 2009 wurde es in das Stockholmer Übereinkommen der weltweit verbotenen Stoffe aufgenommen.[7] Im Jahr 1979 kam es laut einem Bericht des französischen Arztes Dominique Belpomme auf den Bananenplantagen in Martinique und Guadeloupe durch den Einsatz zu einer überdurchschnittlichen Zahl von Prostatakrebs-Fällen und Missbildungen bei neugeborenen Kindern.[8][9]
Analytischer Nachweis
Der chemisch-analytische Nachweis in Umweltproben, Lebens- und Futtermitteln erfolgt nach geeigneter Probenvorbereitung zur Abtrennung der Matrix und gaschromatographischer Abtrennung von Nebenkomponenten mittels hochauflösender massenspektrometrischer Techniken wie der Flugzeitmassenspektrometrie (Time-Of-Flight-Massenspektrometrie).[10]
Weblinks
- Health and Safety Guide (HSG) für Chlordecone
- Persistent Organic Pollutants Toolkit – Chlordecone
- U.S. DEPARTMENT OF HEALTH AND HUMAN SERVICES: Toxicological Profile of Mirex and Chlordecone (PDF; 6,8 MB)
Einzelnachweise
- Eintrag zu Chlordecon in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- Eintrag zu Chlordecone im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Chlordecone in der Pesticide Properties DataBase (PPDB) der University of Hertfordshire, abgerufen am 1. August 2013.
- Philip J. Chenier (2002): Survey of Industrial Chemistry, S. 484.
- Y.-M. Cabidoche, R. Achard, P. Cattan, C. Clermont-Dauphin, F. Massat: Long-term pollution by chlordecone of tropical volcanic soils in the French West Indies: A simple leaching model accounts for current residue. In: Environmental Pollution (= Special Issue Section: Ozone and Mediterranean Ecology: Plants, People, Problems). Band 157, Nr. 5, 1. Mai 2009, S. 1697–1705, doi:10.1016/j.envpol.2008.12.015.
- 13th Report on Carcinogens (RoC): Kepone, abgerufen am 18. November 2014.
- Press Release – COP4 – Geneva, 8 May 2009: Governments unite to step-up reduction on global DDT reliance and add nine new chemicals under international treaty, 2009.
- Welt: Bevölkerung der Antillen von Pestiziden vergiftet.
- Pestizide aus den karibischen Bananenplantagen vergiften Mensch und Natur (Memento vom 10. Juli 2010 im Internet Archive).
- Eric J. Reiner, Adrienne R. Boden, Tony Chen, Karen A. MacPherson und Alina M. Muscalu: Advances in the Analysis of Persistent Halogenated Organic Compounds. In: LC GC Europe. 23 (2010), 60–70.


