Camphersulfonsäure
Camphersulfonsäure, häufig auch als CSA (von englisch Camphorsulfonic acid) abgekürzt, ist eine Organoschwefel-Verbindung und, wie alle Sulfonsäuren, eine relativ starke Säure. Sie ist ein farbloser Feststoff und löslich in vielen organischen Lösungsmitteln.[4] Camphersulfonsäure findet Anwendung als organische Säure aber auch als enantiomerenreine Verbindung zur Racematspaltung von chiralen Aminen und anderen basischen Verbindungen in Form von ihren Salzen.[5] Die (1S)-(+)-Campher-10-sulfonsäure oder deren Ammoniumsalz wird zur Kalibrierung einiger CD-Spektrometer eingesetzt.[6][7]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
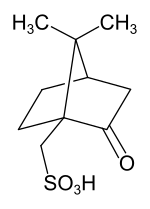 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Camphersulfonsäure | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C10H16O4S | ||||||||||||||||||
| Kurzbeschreibung |
beiger Feststoff mit starkem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 232,3 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
löslich in Wasser[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Synthese
Die Camphersulfonsäure ist kommerziell erhältlich oder durch Sulfonierung von Campher mit Schwefelsäure in Acetanhydrid als Lösungsmittel herstellbar.[4] Der Reaktionsmechanismus verläuft wahrscheinlich nicht über eine direkte Funktionalisierung der unaktivierten Methylgruppe, sondern über mehrere Teilschritte.[8] Protonierung des Ketons induziert eine retro-semi-Pinakol-Umlagerung. Das daraus resultierende Carbokation kann zu einer exo-Methylengruppe deprotoniert werden, welche im nächsten Schritt von einem Elektrophil nicht bekannter Struktur ( oder sind möglich) angegriffen wird. Das resultierende Carbokation reagiert in einer weiteren semi-Pinacol Umlagerung und abschließender Deprotonierung zur Camphersulfonsäure.
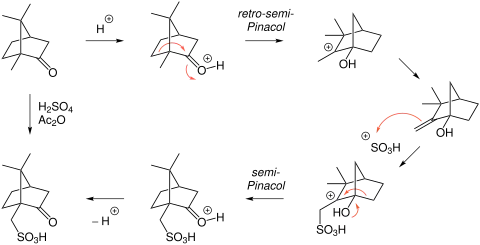
Einzelnachweise
- Eintrag zu CAMPHOR SULFONIC ACID in der CosIng-Datenbank der EU-Kommission, abgerufen am 20. November 2021.
- Eintrag zu Campher-10-sulfonsäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 21. Januar 2020. (JavaScript erforderlich)
- Datenblatt Camphersulfonsäure bei Sigma-Aldrich, abgerufen am 11. Juli 2011 (PDF).
- Paul D. Bartlett, L.H. Knox: D,L-10-Camphorsulfonic Acid (Reychler′s Acid) In: Organic Syntheses. 45, 1965, S. 12, doi:10.15227/orgsyn.045.0012; Coll. Vol. 5, 1973, S. 194 (PDF).
- André B. Charette: 3-Bromocamphor-8-sulfonic Acid. In: Encyclopedia of Reagents for Organic Synthesis 2001, John Wiley & Sons. doi:10.1002/047084289X.rb283
- DeLos F. DeTar: Suggested preliminary standards for calibration of optical rotatory dispersion and circular dichroism instruments. In: Analytical Chemistry. 41, Nr. 11, September 1969, S. 1406–1408. doi:10.1021/ac60280a009.
- G. Chi Chen & Jen Tsi Yang: Two-Point Calibration of Circular Dichrometer with d-10-Camphorsulfonic Acid. In: Analytical Letters. 10, Nr. 14, 1977, S. 1195–1207. doi:10.1080/00032717708067855.
- Reinhard Brückner: Reaktionsmechanismen. Springer Berlin Heidelberg, Berlin, Heidelberg 2004, ISBN 978-3-662-45683-5, doi:10.1007/978-3-662-45684-2.
