Campesterin
Campesterin, auch Campesterol, ist eine Substanz aus der Gruppe der Phytosterine (also der pflanzlichen Sterine) mit der chemischen Formel C28H48O, die ihren Namen erhielt, weil sie erstmals aus der Pflanze Brassica campestris isoliert wurde.[2]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
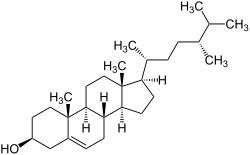 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Campesterin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C28H48O | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 400,68 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Vorkommen
Die Substanz kommt in verschiedenen Pflanzen und Pflanzenteilen vor, wobei der Anteil, in dem sie vorkommt, nicht nur von der Pflanzenart, sondern auch von deren Standort abhängt (bedingt durch Klimaverhältnisse, Bodenbeschaffenheit etc.). Campesterin kommt sowohl in Obst (z. B. Grapefruit, Granatapfel), als auch Gemüse (z. B. Zwiebeln, Gurken) und Getreide (Canola, Hafer, Mais) vor. Außerdem ist es in Löwenzahn und in Gewürzen wie Kardamom, Pfeffer und Zitronengras zu finden. In der Geochemie dient es neben anderen Sterinen als Biomarker in verschiedenen Sedimenten.[3]
Analytik
Zur zuverlässigen qualitativen und quantitativen Bestimmung des Campesterins oder seiner Ester wird nach matrixabhängiger Probenvorbereitung die HPLC-MS[4] oder Kopplung der Gaschromatographie unter Nutzung von Kapillartrennsäulen mit der Massenspektrometrie eingesetzt. Diese Verfahren eignen sich auch zum Nachweis von Fett- oder Ölverfälschungen.[5]
Wirkung
Campesterin hat eine anabole Wirkung auf den Organismus, da es eine steroidartige Vorstufe verschiedener Wachstumshormone darstellt. Es ist wie die meisten Phytosterole in der Lage, LDL und Gesamt-Cholesterin zu senken.[6][7] Ob sich hierdurch eine Senkung des kardiovaskulären Risikos erreichen lässt, ist nicht eindeutig mit Studien belegt. Die Studien, die es dazu gibt, werden in Zweifel gezogen, da es Gegenstudien gibt und die Vermutung naheliegt, dass Menschen, die campesterinreiche Nahrung zu sich nehmen, sich insgesamt gesundheitsbewußter ernähren (mediterrane Kost, hoher Gemüseanteil etc.), so dass eine isolierte Wirkung des Campesterins nicht eindeutig belegbar sei. Möglicherweise besitzt Campesterin eine hemmende Wirkung auf die Resorption von Cholesterin im Darm.[8] Auch hemmt es die Synthese von Cholesterin und Apolipoproteinen.[9]
Wie andere Phytosterine kann auch Campesterin beim Vorliegen einer seltenen Stoffwechselstörung, der Phytosterinämie, zur Ablagerung von phytosterinhaltigen Plaques in den Blutgefäßen beitragen.
Campesterin ist eine Vorstufe des Anabolikums Boldenon, weshalb die Einnahme zu positiven Doping-Testergebnissen führen kann.[10][11][12]
Die Einnahme von Dalcetrapid, einem CETP-Hemmstoff, erhöht die Resorption von Campesterin im Darm.[13]
Wirkung auf andere Nährstoffe
Es wird davon ausgegangen, dass Campesterin die Spiegel verschiedener Mikronährstoffe senkt, nämlich des Vitamin E,[14] der Vitaminvorstufe β-Carotin und des sekundären Pflanzenstoffes Lycopin.[15][16] Wobei sicherlich hinterfragt werden müsste, inwieweit diese Auswirkungen dosisabhängig sind und ob sie bei phytosterinreicher Ernährung oder nur bei Einnahme der isolierten Substanz auftreten. Zumal einige der Nahrungsmittel, die Campesterin enthalten, auch Vitamin E (Kardamom, Granatapfel) oder β-Carotin enthalten.
Einzelnachweise
- Datenblatt Campesterol bei Sigma-Aldrich, abgerufen am 10. Oktober 2012 (PDF).
- W. G. Jing, Z. M. Wang, Y. Zhao, J. Fu, X. L. Zhao, A. Liu: Chemical constituents from seeds of Brassica campestris. In: Zhongguo Zhong Yao Za Zhi. 39(13), Jul 2014, S. 2521–2525. Chinese. PMID 25276975
- G. A. Bataglion, E. Meurer, A. C. de Albergaria-Barbosa, M. C. Bícego, R. R. Weber, M. N. Eberlin: Determination of Geochemically Important Sterols and Triterpenols in Sediments Using Ultrahigh-Performance Liquid Chromatography Tandem Mass Spectrometry (UHPLC-MS/MS). In: Anal Chem. 87(15), 4. Aug 2015, S. 7771–7778. PMID 26132310.
- B. Scholz, N. Menzel, V. Lander, K. H. Engel: An approach based on ultrahigh performance liquid chromatography-atmospheric pressure chemical ionization-mass spectrometry allowing the quantification of both individual phytosteryl and phytostanyl fatty acid esters in complex mixtures. In: J Chromatogr A. 1429, 15. Jan 2016, S. 218–229. PMID 26718186
- H. Zhao, Y. Wang, X. Xu, H. Ren, L. Li, L. Xiang, W. Zhong: Detection of Adulterated Vegetable Oils Containing Waste Cooking Oils Based on the Contents and Ratios of Cholesterol, β-Sitosterol, and Campesterol by Gas Chromatography/Mass Spectrometry. In: J AOAC Int. 98(6), Dez 2015, S. 1645–1654. PMID 26651578
- John W. Farquhar, Maurice Sokolow: Response of Serum Lipids and Lipoproteins of Man to Beta-Sitosterol and Safflower Oil. In: Circulation. Band 17, Nr. 5, 1958, S. 890–899, doi:10.1161/01.CIR.17.5.890, PMID 13537276.
- E. Heggen, L. Granlund, J. I. Pedersen, I. Holme, U. Ceglarek, J. Thiery, B. Kirkhus, S. Tonstad: Plant sterols from rapeseed and tall oils: Effects on lipids, fat-soluble vitamins and plant sterol concentrations. In: Nutrition, Metabolism and Cardiovascular Diseases. Band 20, Nr. 4, 2010, S. 258–265, doi:10.1016/j.numecd.2009.04.001, PMID 19748247.
- S. P. Choudhary, L. S. Tran: Phytosterols: Perspectives in human nutrition and clinical therapy. In: Current Medicinal Chemistry. Band 18, Nr. 29, 2011, S. 4557–4567, doi:10.2174/092986711797287593, PMID 21864283.
- Laura Calpe-Berdiel, Joan Carles Escolà-Gil, Francisco Blanco-Vaca: New insights into the molecular actions of plant sterols and stanols in cholesterol metabolism. In: Atherosclerosis. Band 203, Nr. 1, 2009, S. 18–31, doi:10.1016/j.atherosclerosis.2008.06.026, PMID 18692849.
- G. Gallina, G. Ferretti, R. Merlanti, C. Civitareale, F. Capolongo, R. Draisci, C. Montesissa: Boldenone, Boldione, and Milk Replacers in the Diet of Veal Calves: The Effects of Phytosterol Content on the Urinary Excretion of Boldenone Metabolites. In: J. Agric. Food Chem. 55 (20), 2007, S. 8275–8283.
- M. M. Ros, S. S. Sterk, H. Verhagen, A. F. Stalenhoef, N. de Jong: Phytosterol consumption and the anabolic steroid boldenone in humans: a hypothesis piloted. In: Food Addit Contam. 24(7), Jul 2007, S. 679–684.
- R. Draisci, R. Merlanti, G. Ferretti, L. Fantozzi, C. Ferranti, F. Capolongo, S. Segato, C. Montesissa: Excretion profile of boldenone in urine of veal calves fed two different milk replacers. In: Analytica Chimica Acta. Volume 586, Issues 1–2, 14. March 2007, S. 171–176.
- E. J. Niesor, E. Chaput, A. Staempfli, D. Blum, M. Derks, D. Kallend: Effect of dalcetrapib, a CETP modulator, on non-cholesterol sterol markers of cholesterol homeostasis in healthy subjects. In: Atherosclerosis. Band 219, Nummer 2, Dezember 2011, ISSN 1879-1484, S. 761–767, doi:10.1016/j.atherosclerosis.2011.09.017. PMID 21982411.
- J. Tuomilehto, M. J. Tikkanen, P. Högström, S. Keinänen-Kiukaanniemi, V. Piironen, J. Toivo, J. T. Salonen, K. Nyyssönen, U. H. Stenman, H. Alfthan, H. Karppanen: Safety assessment of common foods enriched with natural nonesterified plant sterols. In: European Journal of Clinical Nutrition. Band 63, Nummer 5, Mai 2009, ISSN 1476-5640, S. 684–691, doi:10.1038/ejcn.2008.11. PMID 18270526.
- Peter Clifton: Lowering cholesterol – A review on the role of plant sterols. In: Australian Family Physician. Band 38, Nr. 4, 2009, S. 218–221, PMID 19350071.
- M. Richelle, M. Enslen, C. Hager, M. Groux, I. Tavazzi, J. P. Godin, A. Berger, S. Métairon, S. Quaile, C. Piguet-Welsch, L. Sagalowicz, H. Green, L. B. Fay: Both free and esterified plant sterols reduce cholesterol absorption and the bioavailability of beta-carotene and alpha-tocopherol in normocholesterolemic humans. In: The American journal of clinical nutrition. Band 80, Nummer 1, Juli 2004, ISSN 0002-9165, S. 171–177. PMID 15213045.
