Bortriazid
Bortriazid (bzw. Triazidoboran) ist eine thermisch instabile Bor-Stickstoff-Verbindung mit einem Stickstoffgehalt von 92,1 %. Formal ist es das Triazidoderivat des Borans. Der Stoff gehört zur Stoffgruppe der kovalenten anorganischen Aziden. Die hochenergetische, zu einer spontanen explosiven Zersetzung neigende Substanz wurde erstmals 1954 von Egon Wiberg und Horst Michaud von der Universität München beschrieben.[1]
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
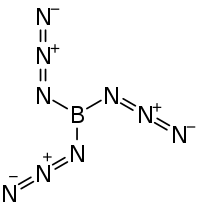 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Bortriazid | ||||||||||||
| Andere Namen |
Triazidoboran | ||||||||||||
| Summenformel | B(N3)3 | ||||||||||||
| Kurzbeschreibung |
farblose Kristalle[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 136,87 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Löslichkeit |
löslich in Diethylether[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Gewinnung und Darstellung
Die erste Herstellung erfolgte durch die Zugabe von Diboran zu einer Lösung von Stickstoffwasserstoffsäure in Diethylether im Temperaturbereich zwischen −20 °C und −10 °C. Die Synthese verläuft über die Zwischenverbindungen Monoazidoboran BH2N3 und Diazidoboran BH(N3)2.[1]
Die Verbindung kann auch durch das Überleiten von Bortribromid-Dampf über festes Silberazid im Hochvakuum erhalten werden.[3]
Eine ähnliche Gasphasensynthese gelingt durch die spontane Umsetzung von Bortrichlorid mit Stickstoffwasserstoffsäure.[4][5]
Eigenschaften
Die Verbindung bildet farblose Kristalle, die nur bei tieferer Temperatur beständig sind. Oberhalb von −35 °C kann ein explosionsartiger Zerfall stattfinden.[1] In der Gasphase erzeugtes Bortriazid zerfällt bei Raumtemperatur innerhalb von 60 Minuten unter Stickstoffabspaltung zu Bornitriden mit der Zusammensetzung BN3 bzw. BN, die sich an der Reaktorwand ablagern. Diese Reaktionen können auch photochemisch durch UV-Licht-Bestrahlung im Absorptionsbereich der Verbindung um 230 nm realisiert werden.[4][5][6]
In Gegenwart von Wasser erfolgt eine Hydrolyse zu Stickstoffwasserstoffsäure und Bortrioxid.[4]
Die Umsetzung mit Aziden, wie Natriumazid oder Lithiumazid ergibt die entsprechenden Tetraazidoboratkomplexe.[1][7]
Die den Tetraazidoboraten zugrundeliegende Tetraazidoborsäure HB(N3)4 kann bei tiefen Temperaturen unterhalb von −60 °C in freiem Zustand erhalten werden.[1]
Verwendung
Eine Verwendung als hochenergetische Substanz ist wegen der geringen Stabilität nicht relevant. Dagegen sind die abgeleiteten Tetraazidoborate oder Addukte mit Basen, wie Chinolin, Pyrazin oder 2,2,6,6-Tetramethylpiperidin dafür eher interessant.[8] Die Verbindung ist als Ausgangsstoff durch Zersetzung aus der Gasphase zur Beschichtung von Oberflächen mit Bornitriden interessant.[4]
Einzelnachweise
- E. Wiberg, H. Michaud: Zur Kenntnis eines Bortriazids. In: Z. Naturforsch. B. Band 9, 1954, S. 497–499. doi:10.1515/znb-1954-0715 (abgerufen über De Gruyter Online).
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- F. Lui, X. Zeng, J. Zhang, L. Meng, S. Zhang, M. Ge, D. Wang, D. Kam Wah Mok, F. Chau: A simple method to generate B(N3)3. In: Chem. Phys. Lett. Band 419, 2006, S. 213–216, doi:10.1016/j.cplett.2005.11.082.
- R. L. Mulinax, G. S. Okin, R. D. Coombe: Gas Phase Synthesis, Structure, and Dissociation of Boron Triazide. In: J. Phys. Chem. Band 99, 1995, S. 6294–6300, doi:10.1021/j100017a007.
- I. A. Al-Jihad, B. Liu, C. J. Linnen, J. V. Gilbert: Gereration of NNBN via Photolysis of B(N3)3 in Low-Temperature Argon Matrices: IR spectra and ab Initio Calculations. In: J. Phys. Chem. A. Band 102, 1998, S. 6220–6226, doi:10.1021/jp9812684.
- M. J. Travers, J. V. Gilbert: UV Absorption Spectra of Intermediates Generated via Photolysis of B(N3)3, BCl(N3)2, and BCl2(N3) in Low-Temperature Argon Matrices. In: J. Phys. Chem. A. Band 104, 2000, S. 3780–3785, doi:10.1021/jp993939j.
- E. Wiberg, H. Michaud: Zur Kenntnis eines ätherlöslichen Lithiumborazids LiB(N3)4. In: Z. Naturforsch. B. Band 9, 1954, S. 499, doi:10.1515/znb-1954-0716 (abgerufen über De Gruyter Online).
- W. Fraenk, T. Habereder, A. Hammerl, T. M. Klapötke, B. Krumm, P. Mayer, H. Nöth, M. Warchhold: Highly Energetic Tetraazidoborate Anion and Boron Triazide Adducts. In: Inorg. Chem. Band 40, 2001, S. 1334–1340, doi:10.1021/ic001119b.
Literatur
- W. Fraenk, T. M. Klapötke: Recent Developments in the Chemistry of Covalent Main Group Azides. In: G. Meyer, D. Naumann, L. Wesemann (Hrsg.): Inorganic Chemistry Highlights. Wiley-VCH Verlag, 2002, ISBN 3-527-30265-4, S. 259–265.