2,2,6,6-Tetramethylpiperidin
2,2,6,6-Tetramethylpiperidin ist eine chemische Verbindung aus der Gruppe der Piperidine.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
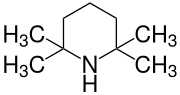 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 2,2,6,6-Tetramethylpiperidin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C9H19N | |||||||||||||||
| Kurzbeschreibung |
klare bis gelbe Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 141,25 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,837 g·cm−3 (25 °C)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
152 °C[2] | |||||||||||||||
| Brechungsindex |
1,445 (20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Gewinnung und Darstellung
Eine Möglichkeit Tetramethylpiperidin 2 darzustellen[3] beginnt mit der Konjugataddition von Ammoniak an Phoron 1. Das Zwischenprodukt Triacetonamin wird in einer Wolff-Kishner-Reaktion reduziert.
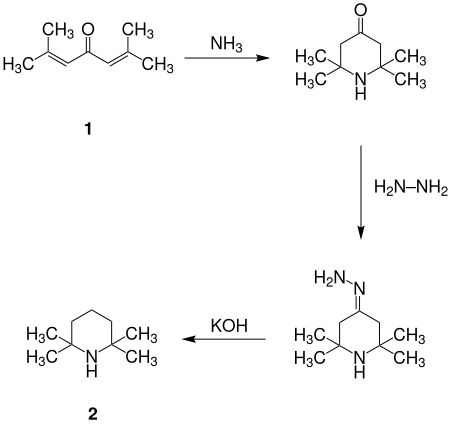
Reaktionsschemata von 2,2,6,6-Tetramethylpiperidin
Verwendung
Tetramethylpiperin bildet die Grundstruktur der HALS-UV-Stabilisatoren (von englisch Hindered Amine Light Stabilizers). Außerdem ist es Grundstoff der Radikalspezies 2,2,6,6-Tetramethylpiperidinyloxyl (TEMPO) und der starken Base Lithiumtetramethylpiperidid.
Einzelnachweise
- Datenblatt bei chemicalland21
- Datenblatt 2,2,6,6-Tetramethylpiperidine, ≥99% bei Sigma-Aldrich, abgerufen am 26. März 2014 (PDF).
- Detlef Kampmann, Georg Stuhlmüller, Roger Simon, Fabrice Cottet, Frédéric Leroux, Manfred Schlosser: A Large-Scale Low-Cost Access to the Lithium 2,2,6,6-Tetramethylpiperidide Precursor. In: Synthesis. 2005, Nr. 06, 2005, S. 1028–1029. doi:10.1055/s-2004-834856.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.

