Biologische Entrostung
Unter biologischer Entrostung versteht man die Entfernung von Rost oder Zunder von metallischen Oberflächen mithilfe biologisch gebildeter Rostumwandler. Die wirksamen Substanzen werden von natürlichen Zellen produziert, die in Lösung gelangen und z. B. Eisen in Komplexbindungen überführen. Diese Substanzen sind Säuren aber auch sogenannte Siderophore (Eisenchelatoren).[1]
Säuren aus mikrobiologischer Produktion
Der chemische Formalismus für die biologische Entrostung ist der gleiche wie bei konventionell hergestellten Säuren. Man unterscheidet in Rostumwandler und Beizmittel. Zu der ersten Gruppe gehört zum Beispiel Phosphorsäure; zu der zweiten Gruppe zählt die Schwefelsäure.
Mikrobielle Herstellung von Phosphorsäure
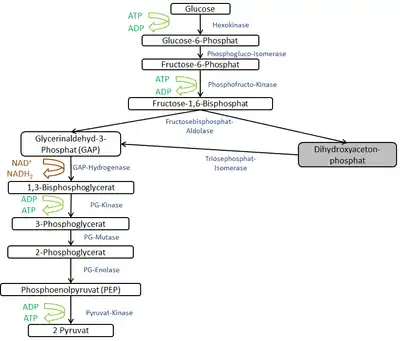
Phosphorsäure kann indirekt über den von Embden, Meyerhof und Parnas beschriebenen Weg (EMP-Weg) produziert werden.[1] Ein wichtiges Zwischenprodukt ist das Fructose-1,6-bisphosphat, weswegen er auch Fructose-Diphosphat-Weg genannt wird.[1] Dieser Weg ist ein Bestandteil der Atmung, bei der organisches Material zu H2O und CO2 unter Energiegewinnung abgebaut wird.[2] Hier wird die Glucose aufgenommen und zu Pyruvat verarbeitet. Daraus resultierende Zwischenprodukte sind phosphorylierte Verbindungen. Eines davon, das Dihydroxyacetonphosphat, kann in einem zweiten Schritt zusammen mit der Phosphatase in Phosphorsäure und Glycerin umgewandelt werden. Untersucht wurde dieser Weg mit Escherichia coli und Clostridium.[1] Da diese auch im Humus vorkommen, wurde auch schon in Versuchen getestet, mit Hilfe von Kompost Oberflächen zu entrosten.[1]
Mikrobielle Herstellung von Schwefelsäure
Mikroorganismen, die aus anorganischer Substanz ihre Energie beziehen, sogenannte chemo-litho-autotrophe Mikroorganismen, verfügen über einen Stoffwechselweg, eisenhaltige Sulfide zu Schwefelsäure zu oxidieren. Die Schwefelsäure ist im Stande, Metalle aus dem Gestein zu lösen. Diesen Prozess nennt man Laugung. Dafür können die Spezies Acidithiobacillus thiooxidans (früher Thiobacillus thiooxidans) und Acidithiobacillus ferrooxidans (früher: Thiobacillus ferrooxidans) eingesetzt werden. Beide Spezies wirken bei den Reaktionen katalytisch. Acidithiobacillus ferrooxidans bildet bei der direkten Laugung aus Eisensulfid das leichter lösliche Eisensulfat sowie Schwefelsäure. Bei der indirekten Laugung werden verschiedene Metallsulfide zu elementarem Schwefel umgesetzt. In einer zweiten Reaktion erzeugt Acidithiobacillus thiooxidans Schwefelsäure. A. thiooxidans arbeitet im Gegensatz zu A. ferroxidans bei sehr niedrigen pH-Werten (2 bis 3). Hohe Ausbeuten an Schwefelsäure lassen sich dadurch erreichen, indem aus beiden Acidithiobacillus-Spezies eine Mischkultur gebildet wird.[1]
Direkte Laugung
Indirekte Laugung
Es gibt weitere Säuren wie Zitronensäure, Weinsäure, Äpfelsäure und Essigsäure, die komplexbildende Eigenschaften haben, jedoch sind die komplexbildenden Eigenschaften nur schwach ausgeprägt. Um die Wirksamkeit der Säuren zu erhöhen, mischt man die Säuren miteinander.[3]
Siderophore
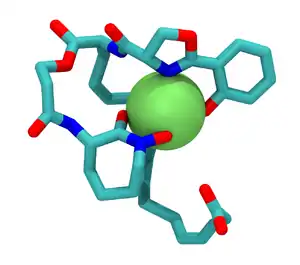
Viele Zellen benötigen Eisen für den Zellaufbau. Da Eisen zwar ein sehr häufiges Element auf der Erde ist, jedoch in physiologischer Lösung (d. h. aerob und pH-Neutral) fast nur in ungelöster Form vorkommt, müssen aerob wachsende Mikroorganismen über eine Strategie verfügen, um an gebundenes Eisen zu gelangen. Bakterien, Pilze und Pflanzen besitzen sog. Siderophore. Siderophore sind selektive Moleküle, die vorwiegend dreiwertiges Eisen binden. Sie gehören der Gruppe der „small molecules“ an. Ihre geringe Größe erlaubt es durch die Zellwand in die Lösung ausgeschieden zu werden, dreiwertiges Eisen aus Eisenverbindungen (z. B. Fe2O3) zu komplexieren und wieder in die Zelle zurückzutransportieren. Die Abbildung zeigt ein an ein Siderophor gebundenes Eisenion (grün).
Nach Reduktion des Fe3+ zu Fe2+ kann das Eisenion vom Siderophor wieder gelöst werden.[1] Siderophore eignen sich übrigens auch zur Entfernung von Aluminiumoxidschichten (Al2O3) zwecks Oberflächenbehandlung.[4] Zum Einsatz kommen diese Siderophore seit etwa Mitte des 20. Jahrhunderts in der Pharmazie gezielt bei der Dialyse und bei Eisenvergiftungen.[1] Die Idee des Einsatzes von Siderophoren zur Entrostung gab es schon Anfang der 90er Jahre.[1] Die Vorteile der Nutzung sind vielfältig. Der größte Vorteil ist jedoch die komplette biologische Abbaubarkeit. Hinzu kommt, dass Siderophore selektiv die Eisenionen der Rostschicht binden und nicht das darunter befindliche Eisen angreifen. Weiterhin sind sie recyclebar und völlig ungiftig.[3] Die Herstellung der Komplexbildner erfolgt in einem stark an Eisen verarmten Milieu, so dass die Mikroorganismen zu einer starken Bildung von Siderophoren angeregt werden. Im Gegensatz zur Pharmazie, kann die Herstellung für eine industrielle Anwendung kostengünstiger erfolgen, da anschließende aufwendige Reinigungsschritte nicht notwendig sind. Es kommen auch nur solche Siderophore in Frage, die in wässriger Umgebung in Lösung gehen. Hierzu besteht eine Patentschrift aus dem Jahre 1994 und beschreibt die Herstellung und den Einsatz von Siderophoren als Entrostungsmittel.[5] Es existieren mittlerweile einige Produkte auf Basis von Siderophoren zur Entrostung von Bauteilen. Diese werden als Zusatzstoff zur Entrostung angeboten und finden Verwendung in kleineren Spülbädern oder als Paste.[6]
Einzelnachweise
- P. M. Kunz: Umweltbioverfahrenstechnik. Vieweg, Braunschweig/ Wiesbaden 1992, ISBN 3-528-06451-X.
- W. Fritsche: Mikrobiologie. 2. Auflage. Spektrum Akademischer Verlag, Heidelberg/ Berlin 1999.
- P. M. Kunz: Natürliche Entrostung. In: Bio World. 1, 2001, S. 8ff.
- P. M. Kunz, A. Hämmerl, I. Sommer: Komplexierung von Aluminiumoxid durch natürliche Chelatoren zur Substitution von Beizsäure beim Glanzbeizen. Feasibility-Studie der Karl-Völker-Stiftung an der Hochschule Mannheim, Februar 2010.
- P. M. Kunz: (1994) Patentschrift DE 4433 376 C1, Abstract: Natürliche Speicher- und Transportverbindungen zur Entrostung von Oberflächen, die in Mikroorganismen vorkommen und das Herstellungsverfahren dieser Verbindungen.
- ASA Spezialenzyme GmbH, aufgerufen am 30. November 2011.