Benfluorex
Benfluorex ist ein Arzneistoff aus der Gruppe der Phenylethylamine, der als Lipidsenker zur Reduktion der Blutfettwerte und zur Gewichtsreduktion beim Diabetes mellitus von Typ II in einigen Ländern, wie beispielsweise in Frankreich, Spanien und Italien, jedoch nicht in Deutschland, zugelassen war. Darüber hinaus wurde Benfluorex häufig als Appetitzügler eingesetzt. Auf Grund eines gehäuften Auftretens von Herzklappenschäden wurde Benfluorex im Jahr 2009 auf Veranlassung der Europäischen Arzneimittelagentur zurückgerufen. Allein in Frankreich werden mindestens 500 Todesfälle in einem möglichen Zusammenhang mit dem Benfluorex-haltigen Arzneimittel Mediator gesehen.[2] Diese Todesfälle sowie das Verhalten der französischen Arzneimittelbehörde Agence française de sécurité sanitaire des produits de santé und des Herstellers Servier führten zum sogenannten Mediator-Skandal.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
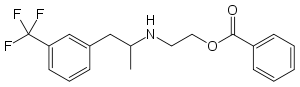 | ||||||||||||||||||||||
| Strukturformel ohne Stereochemie | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Benfluorex | |||||||||||||||||||||
| Andere Namen |
(RS)-2-({1-[3-(Trifluormethyl)phenyl]propan-2-yl}amino)ethylbenzoat | |||||||||||||||||||||
| Summenformel | C19H20F3NO2 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
A10BX06 | |||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 351,4 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Klinische Angaben
Anwendungsgebiete (Indikationen)
Benfluorex war ursprünglich als Lipidsenker zur Behandlung der Hypertriglyceridämie und zur Gewichtsreduktion beim Diabetes mellitus von Typ II in Frankreich und in weiteren Ländern zugelassen worden. Außerhalb der Indikation wurde Benfluorex häufig als Appetitzügler bei Nicht-Typ-II-Diabetikern eingesetzt. Spätestens mit der Beurteilung der Europäischen Arzneimittelagentur besteht für die Anwendung von Benfluorex keine medizinische Indikation mehr.
Unerwünschte Wirkungen (Nebenwirkungen)
Unter der Anwendung von Benfluorex konnten insbesondere unspezifische Nebenwirkungen des Magen-Darm-Systems, wie Übelkeit, Erbrechen, Magenschmerzen und Durchfall, sowie Müdigkeit, Kraftlosigkeit und Schwindel beobachtet werden. In sehr seltenen Fällen traten allergische Reaktionen, Schock, Hypotonie, Hautausschlag, Nesselsucht und Quincke-Ödeme auf. Des Weiteren wurde Benfluorex mit Fällen von erhöhten Leberenzymwerten sowie Fällen von Orientierungs- und Wahrnehmungsstörungen assoziiert.
Benfluorex wurde mit einem gehäuften Auftreten von Herzklappenschäden, sowie mit einer Häufung von Fällen von pulmonaler Hypertonie und Fibrosen des Herzes in Verbindung gebracht. Nach Analyse des französischen Gesundheitsministeriums war der Arzneistoff bei mindestens 500 der etwa 5 Millionen mit dem Medikament Mediator behandelten französischen Patienten möglicherweise für den Tod verantwortlich. Andere Schätzungen gehen von bis zu 2000 Todesfällen in Frankreich aus.[2]
Pharmakologische Eigenschaften
Wirkungsmechanismus (Pharmakodynamik)
Benfluorex gleicht in seiner Wirkweise dem früher ebenfalls als Appetitzügler genutzten und auf Grund von Herzklappenschäden und dem Auftreten von pulmonaler Hypertonie vom Markt genommenen Fenfluramin. Benfluorex wirkt im menschlichen Körper als ein Prodrug, das seine Wirkung nach einer Verstoffwechslung zu dem aktiven Metaboliten Norfenfluramin entfaltet.[3] Dieser Metabolit erhöht zum einen die Freisetzung von Serotonin in den Extrazellularraum und wirkt zum anderen als Agonist an verschiedenen Serotoninrezeptoren, darunter 5-HT2C und 5-HT2B.[4] Während eine Stimulation von 5-HT2C-Rezeptoren mit der appetitzügelnden Wirkung in Verbindung gebracht wird, können die Veränderungen im Bereich des Herzes und der Lungengefäße, welche zu Fibrosen, Herzklappenschäden und pulmonaler Hypertonie führen können, auf eine Aktivierung von 5-HT2B-Rezeptoren zurückgeführt werden.[5]
Entwicklung neuer Arzneien
In den 1960er Jahren suchte das Pharmaunternehmen Servier nach neuen Arzneistoffen auf der Basis der appetitzügelnden Amphetamin. Dieses Projekt führte unter anderem zu den Arzneistoffen Fenfluramin und Benfluorex. 1976 wurde Benfluorex in Frankreich unter dem Namen Mediator auf den Markt gebracht. Darüber hinaus wurde es auch in weiteren europäischen, in asiatischen und afrikanischen Ländern eingesetzt.
Unerwünschte Nebenwirkungen, Verdachtsmeldungen
In den 1980er und 1990er Jahren geriet Fenfluramin im Gegensatz zu Benfluorex auf Grund schwerer Nebenwirkungen, darunter Herzklappenschäden und pulmonale Hypertonie, zunehmend in die Kritik. Der Fenfluramin-Metabolit Norfenfluramin, der später als Ursache dieser Nebenwirkungen identifiziert wurde, war zu diesem Zeitpunkt auch als ein Hauptmetabolit von Benfluorex bekannt.[6] Während Fenfluramin 1997 wegen dieser schweren Nebenwirkungen vom Markt genommen wurde, konnte Mediator in Frankreich nach einem zweimonatigen Ruhen der Zulassung weiter vertrieben werden. Nach dem Rückruf von Fenfluramin setzte man Mediator außerhalb der Zulassung vermehrt als Appetitzügler ein. 1998 ordnete die französische Arzneimittelbehörde ein Überwachungsprogramm für Mediator an. Danach wurden dem Medikament Fälle von Aorteninsuffizienz und pulmonaler Hypertonie zugeschrieben.[7] 2003 wurde erstmals der Wirkstoff in einem direkten Zusammenhang mit Herzklappenschäden gebracht.[8]
In den folgenden Jahren häuften sich Verdachtsberichte, dass Benfluorex, wie auch zuvor für Fenfluramin beobachtet, Herzklappenschäden auslösen kann. Um einem folgenreichen Zulassungswiderruf zu entgehen, verzichtete Servier 2003 auf die fällige Nachzulassung von Mediator in Spanien und Italien. In Deutschland war es nie zugelassen. Als Ergebnis eines Überwachungsprogramms schränkte 2007 die französische Arzneimittelbehörde die Indikationen für Mediator ein. Vom folgenden Jahr an wies die Lungenfachärztin Irène Frachon mehrfach und deutlich auf schwere Nebenwirkungen hin, die sie bei Patienten beobachtet und der Behörde gemeldet hatte. Diese ignorierte solche Hinweise aber. Überdies wandte sich Frachon an Medien. 2010 veröffentlichte sie dazu das Buch Mediator 150 mg: Combien de morts? (Wie viele Tote?) 2009 erfolgte auf Empfehlung der Europäischen Arzneimittelagentur eine Marktrücknahme durch die französische Arzneimittelbehörde. Im folgenden Jahr widerrief die Europäische Arzneimittelagentur schließlich die Zulassung von Mediator.
Gerichtsverfahren
Im September 2019 begann in dieser Sache vor dem Gerichtshof im Pariser Justizpalast das Strafverfahren. Die Anklage wegen fahrlässiger Tötung und Körperverletzung richtet sich gegen 14 Personen und elf Einrichtungen, darunter die Nationale Agentur für Medikamentensicherheit. Geladen wurden 120 Zeugen, zugelassen 376 Anwälte und 4981 Nebenkläger.
Von 1976 bis zum Ende der Zulassung 2009 haben rund fünf Millionen Personen das Mittel eingenommen; Servier erzielte damit einen Umsatz von etwa 500 Millionen Euro. Über 4000 Patienten erlitten schwere Schäden; rund 2000 mussten operiert werden. Man schätzt die Zahl der Verstorbenen als Folge des Mittels auf 1500 bis 2100.
Auf Drängen der französischen Regierung richtete Servier einen Entschädigungsfonds ein, aus dem die Betroffenen bzw. deren Angehörige bisher 135 Millionen Euro erhielten. Zunächst hatte sich das Unternehmen gegen Zahlungen gewehrt. Erst spät räumte es einen Zusammenhang zwischen der Einnahme des Medikaments und den dadurch erlittenen Schäden ein.[9][10]
Am 29. März 2021 wurde Servier wegen schweren Betrugs, fahrlässiger Körperverletzung und fahrlässiger Tötung zu einer Geldstrafe von 2,7 Millionen Euro verurteilt. Der frühere Vizevorsitzende des Konzerns, Jean-Philippe Seta, wurde zusätzlich zu einer Bewährungsstrafe von 4 Jahren verurteilt. Ein Urteil in einem weiteren Prozess steht noch aus.[11]
Literatur
- A. Mullard: Mediator scandal rocks French medical community. In: Lancet. Band 377, Nr. 9769, März 2011, S. 890–892, PMID 21409784.
- I. Frachon: Mediator 150 mg: Combien de morts? édition Dialogues, coll. Ouvertures, Brest 2010, ISBN 978-2-918135-14-2.
Film
- 2016: Die Frau aus Brest (La Fille de Brest) – Regie: Emmanuelle Bercot
Einzelnachweise
- Datenblatt Benfluorex hydrochloride bei Sigma-Aldrich, abgerufen am 10. Oktober 2016 (PDF).
- French judges probe maker of discredited pill. Reuters, 21. September 2011, abgerufen am 10. November 2011.
- K. Boutet, I. Frachon, Y. Jobic u. a.: Fenfluramine-like cardiovascular side-effects of benfluorex. In: Eur. Respir. J. Band 33, Nr. 3, März 2009, S. 684–688, doi:10.1183/09031936.00086308, PMID 19251806.
- L. W. Fitzgerald, T. C. Burn, B. S. Brown u. a.: Possible role of valvular serotonin 5-HT(2B) receptors in the cardiopathy associated with fenfluramine. In: Mol. Pharmacol. Band 57, Nr. 1, Januar 2000, S. 75–81, PMID 10617681.
- R. B. Rothman, M. H. Baumann, J. E. Savage u. a.: Evidence for possible involvement of 5-HT(2B) receptors in the cardiac valvulopathy associated with fenfluramine and other serotonergic medications. In: Circulation. Band 102, Nr. 23, Dezember 2000, S. 2836–2841, PMID 11104741.
- B. H. Gordon: The pharmacokinetics of the metabolites of benfluorex in chronic administration [...] in human volunteers Servier Report No. 93-5792-001. 1993. (lefigaro.fr, PDF; 1,2 MB).
- Eric Favereau: Mediator, coupe-faim dangereux et longtemps toléré. In: Libération. 16. November 2010 (liberation.fr).
- J. Rafel Ribera, R. Casañas Muñoz, N. Anguera Ferrando, N., Batalla Sahún, A. Castro Cels, R. Pujadas Capmany: Valvular heart disease associated with benfluorex. In: Rev Esp Cardiol. Band 56, Nr. 2, Februar 2003, S. 215–216, PMID 12605770 (spanisch, revespcardiol.org).
- R. Klingsieck: Ärztin deckte Skandal auf. In Frankreich findet ein Megaprozess gegen den Pharmakonzern Servier und die Aufsichtsbehörde für Medikamente statt. In: Neues Deutschland. 1. Oktober 2019, S. 7. (neues-deutschland.de)
- R. Balmer: Französischer Heilmittelskandal vor Gericht. 24. September 2019. (nzz.ch)
- In: france24 29. März 2021