2,5-Hexandiol
2,5-Hexandiol ist eine chemische Verbindung aus der Gruppe der Diole und bildet drei Stereoisomere:
- (2R,5R)-2,5-Hexandiol,
- (2S,5S)-2,5-Hexandiol und
- meso-2,5-Hexandiol.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
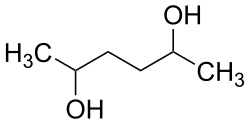 | ||||||||||||||||
| Vereinfachte Strukturformel ohne Stereochemie | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 2,5-Hexandiol | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H14O2 | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 118,18 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
0,96 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
221 °C[1] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,447 (20 °C)[4] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Gewinnung und Darstellung
(2R,5R)-Hexandiol kann aus 2,5-Hexandion gewonnen werden.[5][6]
Eigenschaften
2,5-Hexandiol ist eine brennbare, schwer entzündbare, farblose Flüssigkeit, die leicht löslich in Wasser ist.[1]
Verwendung
2,5-Hexandiol kann zur Herstellung anderer chemischer Verbindungen z. B. 2,4-Hexadien[7] verwendet werden.[8] (2S,5S)-2,5-Hexandiol ist eine Vorstufe chiraler Phosphin-Katalysatoren und chiraler pharmazeutischer Zwischenprodukte.[9]
Einzelnachweise
- Eintrag zu CAS-Nr. 2935-44-6 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Oktober 2016. (JavaScript erforderlich)
- J. Buckingham: Dictionary of Organic Compounds. CRC Press, 1986, ISBN 978-0-412-54090-5, S. 3511 (eingeschränkte Vorschau in der Google-Buchsuche).
- William M. Haynes: CRC Handbook of Chemistry and Physics, 94th Edition. CRC Press, 2016, ISBN 978-1-4665-7115-0, S. 298 (eingeschränkte Vorschau in der Google-Buchsuche).
- Datenblatt 2,5-Hexanediol, 99% (mixture of isomers) bei Sigma-Aldrich, abgerufen am 8. Oktober 2016 (PDF).
- Jürgen Haberland, Werner Hummel, Thomas Daussmann, Andreas Liese: New Continuous Production Process for Enantiopure (2 R ,5 R )-Hexanediol. In: Organic Process Research & Development. Band 6, Nr. 4, Juli 2002, ISSN 1083-6160, S. 458–462, doi:10.1021/op020023t (acs.org [abgerufen am 5. Juni 2021]).
- J. Haberland, A. Kriegesmann, E. Wolfram, W. Hummel, A. Liese: Diastereoselective synthesis of optically active (2R,5R)-hexanediol. In: Applied Microbiology and Biotechnology. 58, 2002, S. 595, doi:10.1007/s00253-002-0936-5.
- Externe Identifikatoren von bzw. Datenbank-Links zu 2,4-Hexadien: CAS-Nummer: 5194-51-4, EG-Nummer: 225-980-9, ECHA-InfoCard: 100.023.619, PubChem: 638071, ChemSpider: 553634, Wikidata: Q27270785.
- Eberhard Breitmaier, Günther Jung: Organische Chemie Grundlagen, Stoffklassen, Reaktionen, Konzepte, Molekülstrukturen ; 129 Tabellen. Georg Thieme Verlag, 2005, ISBN 978-3-13-541505-5, S. 86 (eingeschränkte Vorschau in der Google-Buchsuche).
- M. Bertau, M. Katzberg, W. Hummel, T. Daußmann, J. Stohrer: Biokatalytische Synthese von (S,S)-2,5-Hexandiol. In: Chemie Ingenieur Technik. 78, 2006, S. 1437, doi:10.1002/cite.200650458.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.
