2,3,3-Trimethylindolenin
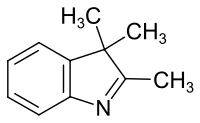
2,3,3-Trimethylindolenin ist eine chemische Verbindung mit einem isomeren Indol-Gerüst (2H-Indol) und drei Methylgruppen als Substituenten. Die Synthese aus dem Phenylhydrazon des Methylisopropylketon (3-Methylbutanon) wurde 1898 von Giuseppe Plancher beschrieben.[2]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2,3,3-Trimethylindolenin | ||||||||||||||||||
| Andere Namen |
2,3,3-Trimethyl-3H-indol | ||||||||||||||||||
| Summenformel | C11H13N | ||||||||||||||||||
| Kurzbeschreibung |
gelb bis braune, brennbare Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 159,23 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
0,992 g·cm−3 (25 °C)[1] | ||||||||||||||||||
| Schmelzpunkt |
6–8 °C[1] | ||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit |
schwer löslich in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
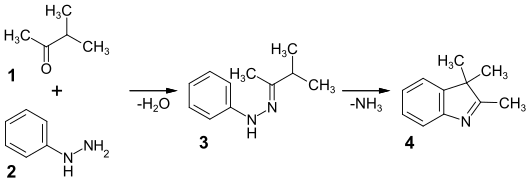
2,3,3-Trimethylindolenin erhält man durch eine Fischer-Indol-Synthese, indem man 3-Methylbutanon 1 mit Phenylhydrazin 2 zu dem Phenylhydrazon 3 umsetzt und anschließend unter Abspaltung von Ammoniak zu 4 cyclisiert.[3]
Verwendung
Durch Methylierung von 2,3,3-Trimethylindolenin 1 mit Dimethylsulfat 2 ist über das 1,2,3,3-Tetramethyl-3H-indolium-Salz 3 die Fischer-Base 4 zugänglich. Diese wiederum ist ein Ausgangsprodukt von Polymethinfarbstoffen.[3]
.svg.png.webp)
Einzelnachweise
- Eintrag zu 2,3,3-Trimethylindolenin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- G. Plancher: Ueber die Methylirung der Indole. In: Berichte der deutschen chemischen Gesellschaft. Band 31, Nr. 2, 1898, S. 1488–1499, doi:10.1002/cber.18980310238 (bnf.fr).
- Eberhard Breitmaier, Günther Jung: Organische Chemie. Grundlagen, Stoffklassen, Reaktionen, Konzepte, Molekülstruktur. 5. Auflage. Georg Thieme Verlag, Stuttgart 2005, ISBN 3-13-541505-8, S. 718 (eingeschränkte Vorschau in der Google-Buchsuche).
